從原發竈脫離的第N天之後,在血液中(zhōng)曆經九九八十一難的癌細胞大軍,僅有(yǒu)萬分(fēn)之二的癌細胞還活着。
突然,傳出了一段若隐若現的對話。
癌細胞:咦?我感覺我們好像到肝了。
肝細胞:好像是癌細胞來了。
癌細胞:肝細胞,是你們嗎?我是癌細胞。
肝細胞:是的!癌細胞,你們終于到了!兄弟(dì)們快接客。
癌細胞:兄弟(dì)們,可(kě)以蘇醒啦,可(kě)以安(ān)營紮寨啦!
在一片歡呼聲中(zhōng),長(cháng)途跋涉而來的癌細胞在肝髒裏紮根了、壯大了。
(以上内容,純屬虛構;如有(yǒu)雷同,純屬鬼扯。)
今天,由瑞士蘇黎世聯邦理(lǐ)工(gōng)學(xué)院Andreas E. Moor領銜的研究團隊,在頂級期刊《自然》上發表一項重磅研究成果,于是就有(yǒu)了上面那部分(fēn)内容。
Moor團隊發現,脫離原發竈的腸癌、胰腺癌和黑色素瘤等癌細胞,細胞表面往往有(yǒu)很(hěn)多(duō)信号素semaphorin,這種信号素蛋白會與正常肝細胞表面的神經叢蛋白plexin B2結合;二者的結合會給癌細胞釋放一個重要的信号:是時候從有(yǒu)利于轉移的上皮-間充質(zhì)轉化(EMT)狀态,逆轉到有(yǒu)利于定殖的間充質(zhì)-上皮轉化(MET)狀态了[1]。最終實現了癌症的肝轉移。
簡單來說,Moor團隊這項研究揭示了遠(yuǎn)處轉移的癌細胞确定轉移竈并啓動轉移竈形成的機制。不難看出,這一發現對于癌症轉移的預防有(yǒu)重要意義。此外,它還填補了癌症轉移的“種子與土壤”假說的關鍵空白。
▲ 論文(wén)首頁(yè)截圖
轉移是癌症導緻患者死亡的罪魁禍首。
然而,我們對癌症的轉移仍缺乏全面的認知。
雖然“種子與土壤”假說已經提出近150年了,但是大多(duō)數的研究集中(zhōng)在“種子”本身或者“種子”遠(yuǎn)程調節“土壤”的機制上。至于“土壤”是否以及如何影響“種子”癌細胞的狀态和命運,從而促進或阻礙轉移竈的形成,目前仍無人知曉[2]。
作(zuò)為(wèi)研究體(tǐ)内細胞相互作(zuò)用(yòng)的專家,Andreas E. Moor想搞清楚進入肝髒的癌細胞是如何與肝髒細胞互動,并最終形成轉移竈的。
為(wèi)此,他(tā)們設計了一種可(kě)以揭示體(tǐ)内細胞與細胞間相互作(zuò)用(yòng)的實驗技(jì )術——CRISPR調節的轉錄激活(CRISPR-a)。還提出了一個假設:接種癌細胞之後,與過表達促轉移因子的肝細胞相互作(zuò)用(yòng)的癌細胞會形成轉移竈,而與過表達抑制轉移因子的肝細胞相互作(zuò)用(yòng)的癌細胞無法形成轉移竈。
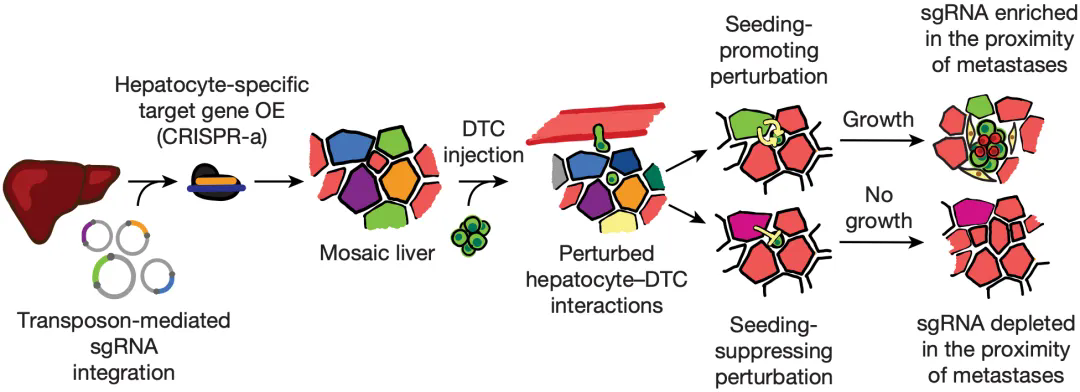
▲ CRISPR-a技(jì )術流程
在CRISPR-a技(jì )術和上述假設的支持下,Moor團隊開始大規模的篩選工(gōng)作(zuò)。最終,他(tā)們發現肝細胞表達的神經叢蛋白plexin B2能(néng)直接與癌細胞相互作(zuò)用(yòng)。
在小(xiǎo)鼠肝髒中(zhōng)過表達plexin B2的編碼基因Plxnb2,會導緻轉移竈的數量增加3倍,而且這種促進作(zuò)用(yòng)在腸癌、胰腺癌和黑色素瘤的轉移實驗中(zhōng)均有(yǒu)體(tǐ)現。
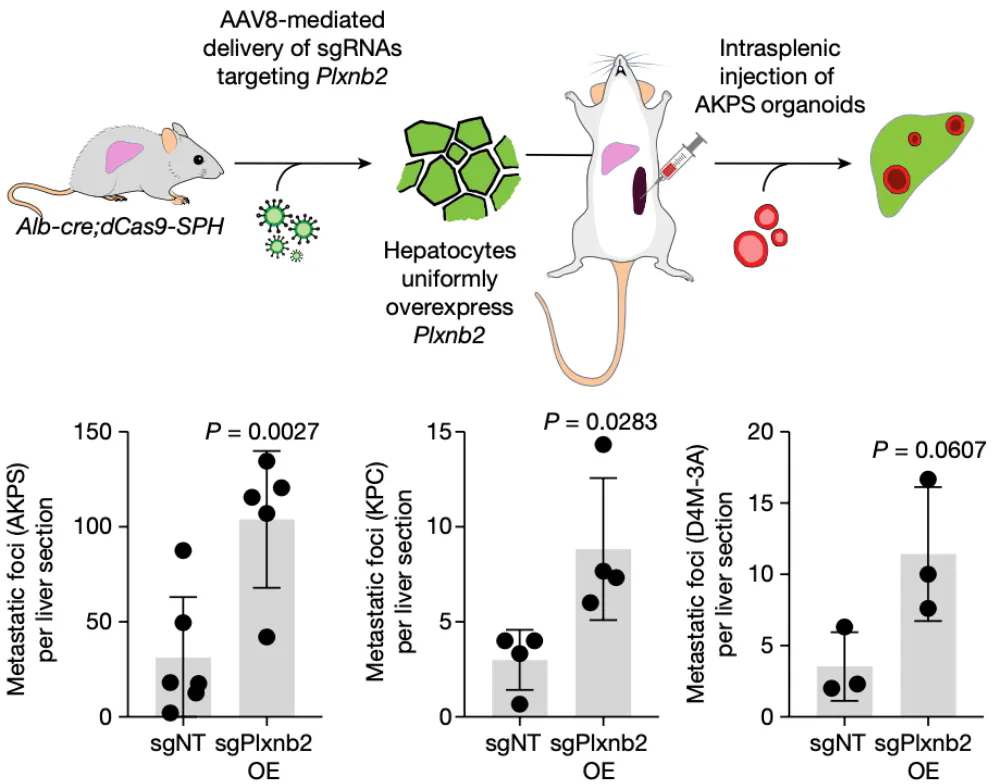
▲ 過表達Plxnb2會促進腸癌(AKPS)、胰腺癌(KPC)和黑色素瘤(D4M-3A)轉移
為(wèi)了展現plexin B2促轉移的能(néng)力,Moor團隊還做了一組數據。
Plxnb2基因過表達小(xiǎo)鼠接種腸癌細胞系(AKPS)之後,86%的小(xiǎo)鼠會形成自發肝轉移竈;而Plxnb2基因正常表達小(xiǎo)鼠這一數據為(wèi)29%。值得注意的是,如果敲除Plxnb2基因的話,即使接種轉移潛力更強悍的腸癌細胞系(APTAK),轉移竈形成率也會暴跌。
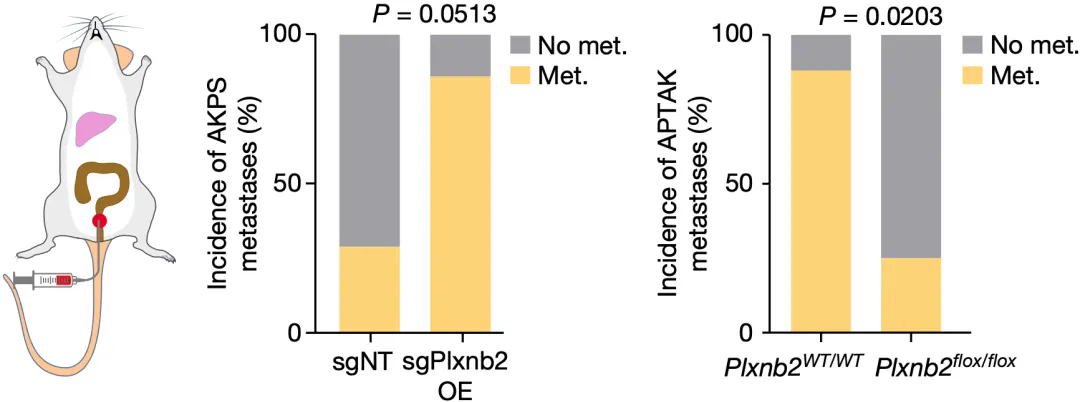
▲ plexin B2有(yǒu)強大的促轉移能(néng)力
随後基于組織學(xué)的研究讓Moor團隊發現,轉移率增加不是由Plxnb2過表達導緻的肝髒環境改變引起的,而是由癌細胞與肝細胞的直接相互作(zuò)用(yòng)引起的。
如果是這樣的話,肝細胞與癌細胞的接觸,到底給癌細胞帶來了哪些變化呢(ne)?
測序結果顯示,在Plxnb2過表達的肝髒中(zhōng),癌細胞裏的KLF4水平升高。KLF4會抑制上皮-間充質(zhì)轉化(EMT),而上皮-間充質(zhì)轉化是癌症轉移的重要條件,因此在轉移性癌細胞中(zhōng),KLF4的水平往往比較低。
既然KLF4水平升高,說明上皮-間充質(zhì)轉化肯定要被抑制。要是上皮-間充質(zhì)轉化被KLF4抑制并逆轉為(wèi)間充質(zhì)-上皮轉化(MET)的話,就會促進癌細胞從轉移階段切換到增殖階段。
基于細胞生物(wù)學(xué)和轉錄組學(xué)數據,Moor團隊證實,進入Plxnb2過表達肝髒的癌細胞,确實從上皮-間充質(zhì)轉化(EMT)逆轉為(wèi)間充質(zhì)-上皮轉化(MET),而且癌細胞也确實進入了快速增殖狀态。
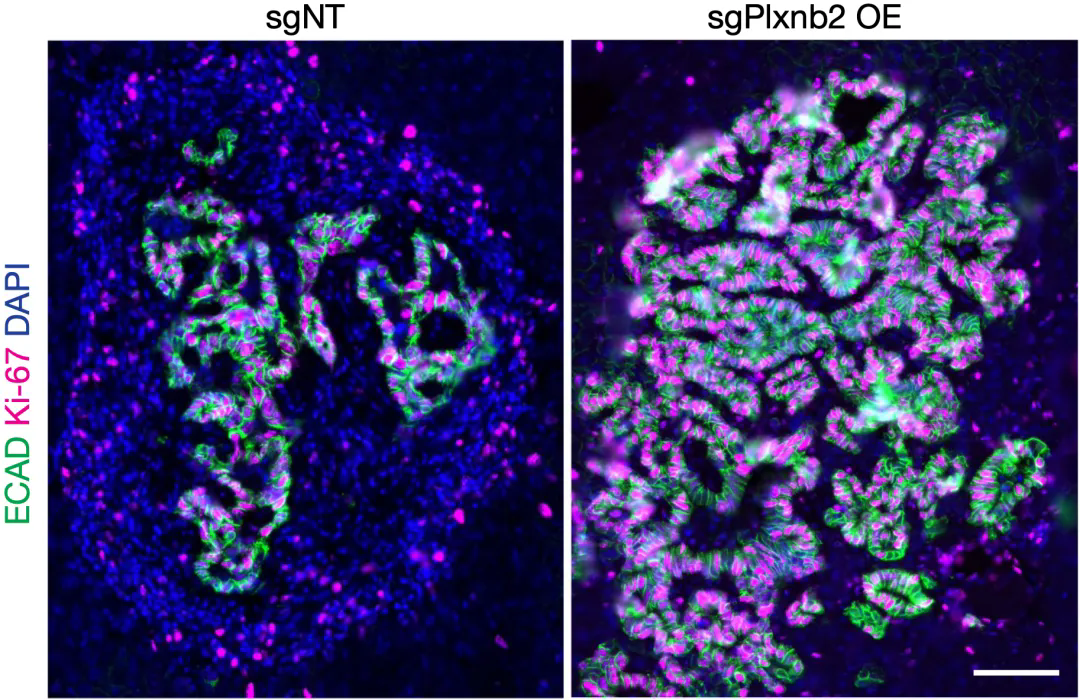
▲ Plxnb2過表達肝髒中(zhōng),癌細胞的增殖明顯更活躍
在研究的最後,Moor團隊證實,肝細胞的plexin B2是通過與癌細胞上的配體(tǐ)IV類semaphorins結合,發揮促進癌症轉移作(zuò)用(yòng)的。
将上面的分(fēn)子機制整合起來,我們就可(kě)以發現肝細胞幫助癌細胞啓動轉移竈形成的過程。表面有(yǒu)semaphorins的癌細胞進入肝髒之後,一旦與表面有(yǒu)plexin B2的肝細胞結合,就會導緻癌細胞的KLF4水平升高,癌細胞就會從轉移模式切換到增殖模式,構建轉移竈。
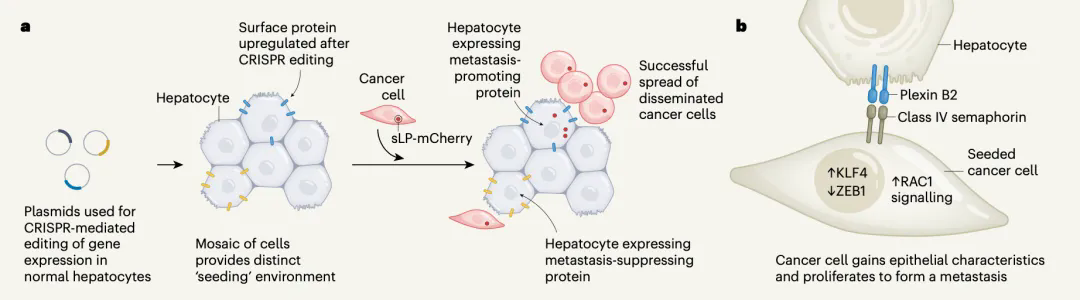
▲ 機制示意圖
好消息是,Moor團隊還發現,抑制肝細胞中(zhōng)plexin B2的表達,或敲除癌細胞中(zhōng)IV類semaphorins的編碼基因,就可(kě)以阻斷肝細胞和癌細胞之間的相互作(zuò)用(yòng),幾乎能(néng)完全抑制肝轉移竈的形成。
這也意味着,Moor團隊的這項研究成果為(wèi)開發預防癌症轉移的藥物(wù)提供了潛在靶點。
參考文(wén)獻:
[1].Borrelli, C., Roberts, M., Eletto, D. et al. In vivo interaction screening reveals liver-derived constraints to metastasis. Nature (2024). https://doi.org/10.1038/s41586-024-07715-3
[2].https://www.nature.com/articles/d41586-024-02235-6
----------THE END----------免責聲明:本文(wén)系轉載分(fēn)享,文(wén)章觀點、内容、圖片及版權歸原作(zuò)者所有(yǒu),如涉及侵權請聯系删除!