在我們的腸道中(zhōng),微生物(wù)群通過合作(zuò)和競争機制維持平衡,一旦失調便會發生有(yǒu)害微生物(wù)的異常增殖,持續毒性代謝(xiè)産(chǎn)物(wù)。腸道微生物(wù)的生态失衡,甚至可(kě)以影響到遙遠(yuǎn)的中(zhōng)控系統,也就是我們的大腦。
近日,葡萄牙科(kē)英布拉大學(xué)的Nuno Empadinhas、Sandra Morais Cardoso等人發表在Molecular Neurodegeneration期刊上的最新(xīn)研究揭示,帕金森病(PD)患者的腸道菌群失調可(kě)能(néng)通過“腸-腦軸”影響大腦健康。
研究發現,将帕金森病患者的腸道微生物(wù)移植給野生型小(xiǎo)鼠後,小(xiǎo)鼠在數周内會出現腸道炎症和α-突觸核蛋白聚集,并進一步發展為(wèi)系統性炎症和腸道屏障損傷,伴随中(zhōng)腦黑質(zhì)區(qū)域多(duō)巴胺能(néng)神經元的損傷和線(xiàn)粒體(tǐ)功能(néng)障礙。
研究還提出,終末回腸的aSyn聚集水平與系統性炎症相關,或可(kě)作(zuò)為(wèi)帕金森病的早期生物(wù)标志(zhì)物(wù)。
這些結果支持了“始于腸道”的病理(lǐ)假說,認為(wèi)帕金森病的病變可(kě)能(néng)從腸道逐步向大腦擴散,為(wèi)以腸道微生物(wù)為(wèi)靶點的帕金森病幹預策略提供了新(xīn)思路。

論文(wén)首頁(yè)截圖
Braak及其同事曾提出假設,指出帕金森病的病理(lǐ)變化起源于腸道神經系統,并通過整個胃腸道傳遞至大腦。這一假說認為(wèi),來自腸道微生物(wù)的毒素或病原體(tǐ)可(kě)能(néng)通過迷走神經逆向傳播,從而在中(zhōng)樞神經系統中(zhōng)引發帕金森病病變。臨床上,帕金森病患者在運動症狀出現之前常伴有(yǒu)胃腸道症狀,這支持了腸道在疾病早期可(kě)能(néng)發揮着重要作(zuò)用(yòng);此外,迷走神經幹切斷術可(kě)以顯著降低患病風險,也為(wèi)帕金森病的腦-腸軸機制增添了信服力。
已被證實的是,帕金森病患者的腸道菌群與健康人群确實存在顯著差異,其中(zhōng)的具(jù)體(tǐ)作(zuò)用(yòng)機制仍在不斷揭秘之中(zhōng)。
在這項研究中(zhōng),研究者們首先對44名(míng)帕金森病患者和21名(míng)健康參與者的糞便樣本進行高通量測序,确定患者腸道微生物(wù)的多(duō)樣性及特征。結果顯示,帕金森病患者的腸菌中(zhōng)乳酸杆菌和鏈球菌豐度顯著增多(duō),糞杆菌顯著減少。
為(wèi)了驗證帕金森病相關失調菌群的作(zuò)用(yòng),研究者們将從帕金森病患者和健康參與者采集的糞便移植到野生型小(xiǎo)鼠體(tǐ)内。
糞菌移植後,小(xiǎo)鼠體(tǐ)重和血糖水平保持穩定,均未出現焦慮或記憶功能(néng)的改變。但在一系列行為(wèi)測試中(zhōng),移植帕金森病患者糞便的小(xiǎo)鼠表現出帕金森病特有(yǒu)的運動功能(néng)缺陷,包括平衡杆測試中(zhōng)的運動障礙、後肢攀爬評分(fēn)升高、抓握測試耐力下降,以及氣味辨識障礙,這些均未在移植健康對照菌群的小(xiǎo)鼠中(zhōng)觀察到。
另外,組織學(xué)分(fēn)析顯示,移植帕金森病患者糞菌的小(xiǎo)鼠在黑質(zhì)區(qū)域的多(duō)巴胺神經元減少約30%,紋狀體(tǐ)中(zhōng)多(duō)巴胺水平下降約52%。
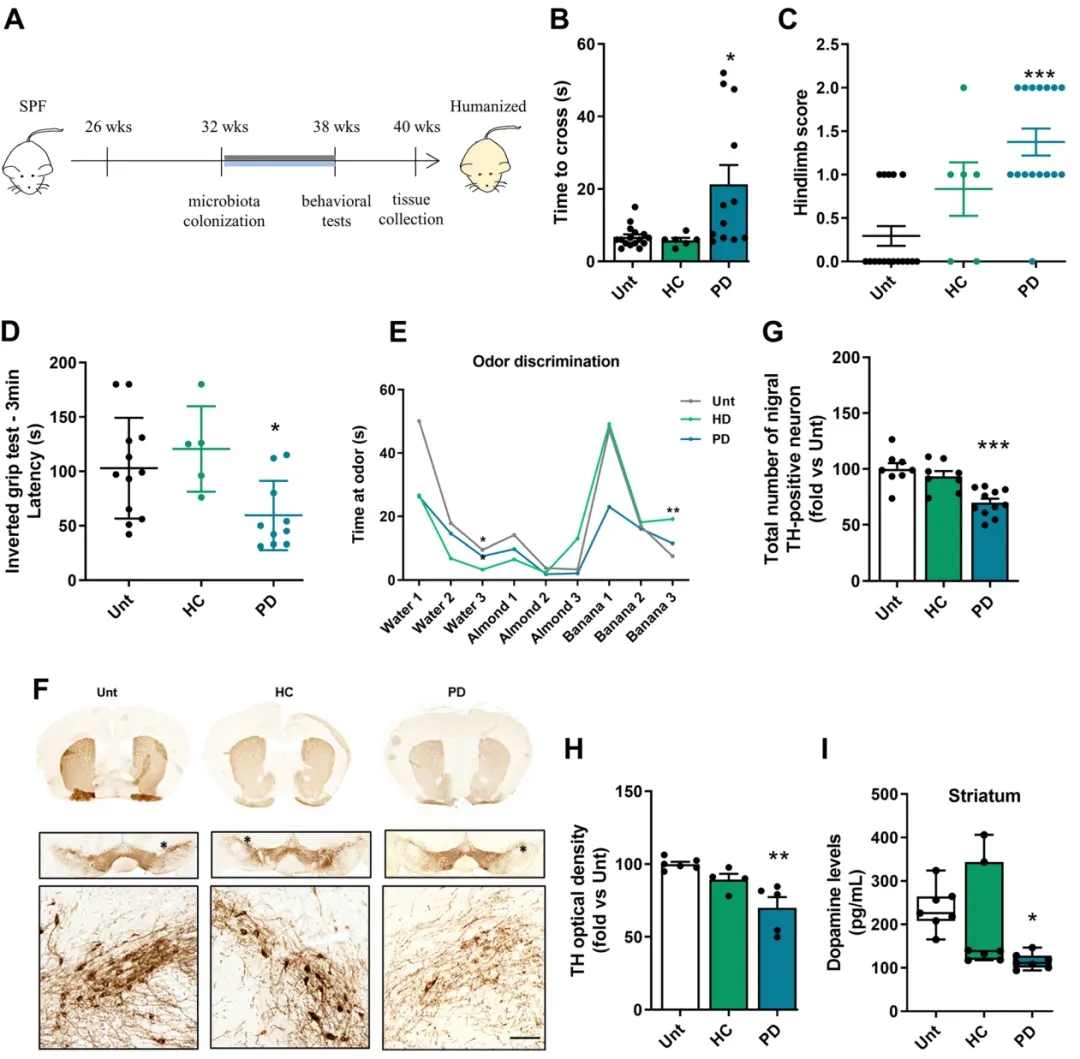
給野生型小(xiǎo)鼠移植帕金森病患者腸菌
測序結果表明,接受帕金森病患者糞菌移植的小(xiǎo)鼠回腸黏膜菌群結構發生改變。不僅如此,帕金森病相關菌群的定植,還導緻小(xiǎo)鼠的腸道發生炎症反應、腸道屏障受損,血液中(zhōng)CD4+T細胞減少、CD8+T細胞增加,TNF、IL-6等促炎細胞因子的表達升高。
除了會加劇小(xiǎo)鼠系統性炎症反應,研究者們發現,帕金森病患者來源的腸菌還會破壞小(xiǎo)鼠的大腦屏障,導緻黑質(zhì)區(qū)域的微血管滲漏增加。
更重要的是,他(tā)們在接受帕金森病患者糞菌移植的小(xiǎo)鼠中(zhōng)觀察到,腸道屏障的損害加劇了α-突觸核蛋白(aSyn)在腸道中(zhōng)的聚集。α-突觸核蛋白(aSyn)的聚集是帕金森病的重要病理(lǐ)特征。不僅僅是在腸道,研究者們在這些小(xiǎo)鼠的迷走神經的背側運動核(DMV)和中(zhōng)腦區(qū)域,也檢測到病理(lǐ)性aSyn的聚集,這支持了Braak假說中(zhōng)aSyn經迷走神經向大腦擴散的可(kě)能(néng)性。
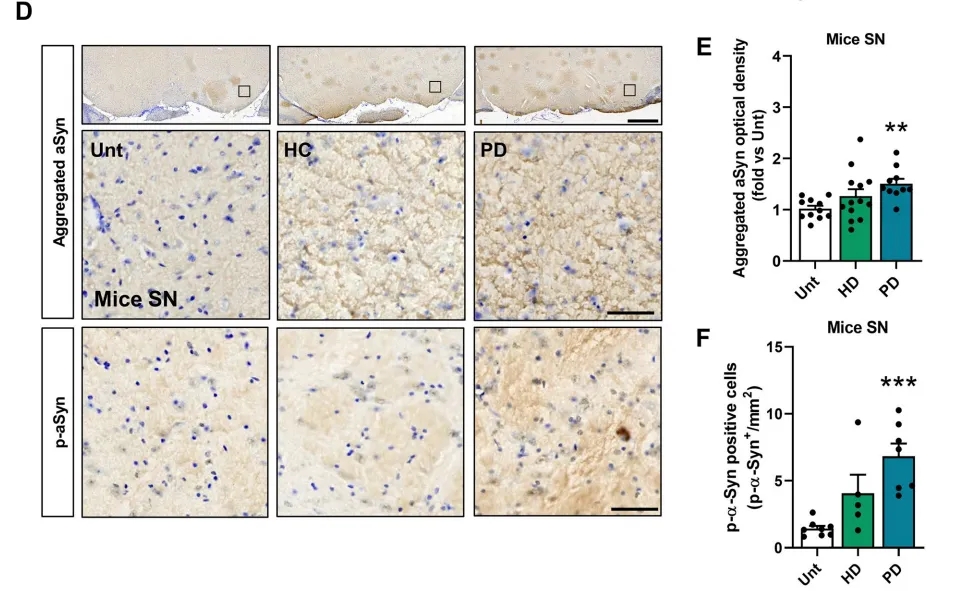
在中(zhōng)腦區(qū)域檢測到病理(lǐ)性aSyn的聚集
進一步研究結果顯示,這些小(xiǎo)鼠的中(zhōng)腦黑質(zhì)區(qū)域的線(xiàn)粒體(tǐ)碎片化增加,且與病理(lǐ)性aSyn水平相關,表現為(wèi)ATP合成減少,線(xiàn)粒體(tǐ)功能(néng)受損。
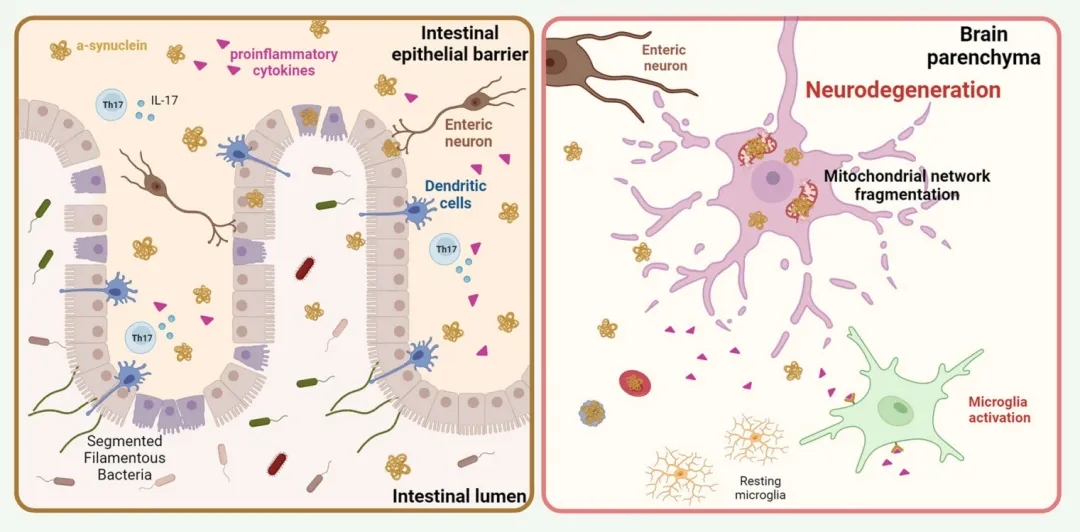
線(xiàn)粒體(tǐ)碎片化後暴露心磷脂,激活免疫反應,導緻神經退行性病變。具(jù)體(tǐ)而言,研究者們在帕金森病患者和糞菌移植小(xiǎo)鼠模型的病理(lǐ)樣本中(zhōng)均觀察到,中(zhōng)腦區(qū)域的TLR4和NFkB通路活化,促使IL-1β表達和促炎免疫通路激活。同時,PD小(xiǎo)鼠和患者的黑質(zhì)區(qū)域中(zhōng)IL-8和IL-17水平升高,進一步破壞血腦屏障的完整性。激活的小(xiǎo)膠質(zhì)細胞釋放TNF和IL-1β,加劇血腦屏障滲漏,使外周免疫細胞更易進入中(zhōng)樞神經系統,進一步推動帕金森病的病變進展。
為(wèi)驗證這些結果,研究者們制定了糞菌移植方案,按照第一周每日移植、随後每周兩次的方式将帕金森病患者的糞便連續六周移植到野生型小(xiǎo)鼠中(zhōng),以強制性引發小(xiǎo)鼠的腸道失調,從而模拟帕金森病的慢性病變過程。
結果顯示,移植後3周,小(xiǎo)鼠出現明顯的腸道炎症,伴有(yǒu)回腸區(qū)域的aSyn聚集;4周後,系統性炎症和腸道屏障滲漏相繼出現;在36周時,小(xiǎo)鼠的運動功能(néng)和中(zhōng)腦多(duō)巴胺能(néng)神經元保持穩定,中(zhōng)腦區(qū)域仍未見aSyn聚集。這表明帕金森病的病理(lǐ)可(kě)能(néng)從腸道逐步傳播到腦部,并需一定時間和推動因素使病變擴散至大腦,證明了“始于腸道”的病理(lǐ)機制存在。
G、H:3周後aSyn在腸道聚集;J:4周後發生系統性炎症;M、N、K、L:36周時多(duō)巴胺能(néng)神經元穩定,運動行為(wèi)未改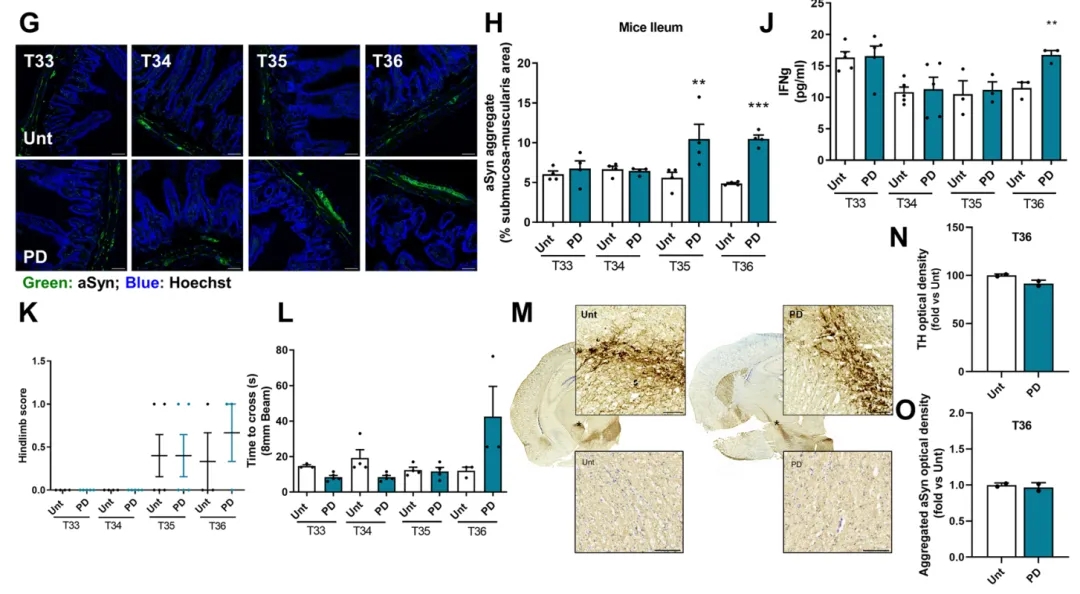 變
變
先前已有(yǒu)研究發現,移植帕金森病患者的腸道菌群會加速遺傳小(xiǎo)鼠模型的病理(lǐ)學(xué)進展,但尚未研究其對野生型小(xiǎo)鼠的影響。此次研究結果表明,帕金森病患者的腸道菌群可(kě)能(néng)産(chǎn)生毒素物(wù)質(zhì),轉移到野生型小(xiǎo)鼠體(tǐ)内會建立一條有(yǒu)害的“腸-腦”傳播途徑,誘導帕金森樣行為(wèi)、組織病理(lǐ)學(xué)特征和多(duō)巴胺能(néng)神經變性。未來應進一步探索,腸道抗炎藥物(wù)是否有(yǒu)助于緩解腸道病變并延緩帕金森病理(lǐ)向大腦的擴散。
----------THE END----------免責聲明:本文(wén)系轉載分(fēn)享,文(wén)章觀點、内容、圖片及版權歸原作(zuò)者所有(yǒu),如涉及侵權請聯系删除!