基因治療是指将外源正常基因導入靶細胞,以糾正或補償缺陷和異常基因引起的疾病,達到治療目的。基因治療的爆發起源于20世紀90年代初,随着人類對基因治療的認識不斷加深,基因療法也愈來愈成熟,經過三十幾年科(kē)學(xué)技(jì )術的發展,全球的基因治療行業已經大步邁向成長(cháng)期,在某些适應證上基因治療已經比傳統的治療方案更加有(yǒu)優勢。
2019年5月,全球首個治療輸血依賴型β地中(zhōng)海貧血(TDT)的基因療法Zynteglo(LentiGlobin,bb1111,含βA-T87Q珠蛋白編碼基因的自體(tǐ)CD34+細胞)獲得歐洲藥品管理(lǐ)局(EMA)有(yǒu)條件批準,其研發公(gōng)司為(wèi)藍鳥生物(wù)公(gōng)司(bluebird bio)。Zynteglo是一種一次性基因療法,開發用(yòng)于治療β 地中(zhōng)海貧血和鐮狀細胞病(SCD)。2020年9月,EMA已授予Zynteglo治療SCD的優先藥物(wù)資格(PRIME),此前,EMA還授予了Zynteglo治療SCD的孤兒藥資格(ODD);在美國(guó),FDA授予了Zynteglo治療SCD的ODD、快速通道資格(FTD)、再生醫(yī)學(xué)先進療法資格(RMAT)、罕見兒科(kē)疾病資格(RPDD)。
目前,LentiGlobin基因療法用(yòng)于治療SCD正處于臨床研究階段,臨床開發計劃包括已完成的1/2期HGB-205研究、正在進行的1/2 期(HGB-206)和3期(HGB-210)臨床研究。但這個适應症的開發過程就沒有(yǒu)β 地中(zhōng)海貧血那麽順利,2021年2月16日,藍鳥生物(wù)宣布停止基因療法LentiGlobin治療SCD的1/2期和3期臨床研究,原因是參加其基因療法LentiGlobin1/2 期(HGB-206)臨床試驗的SCD患者中(zhōng)分(fēn)别出現一例患急性髓細胞白血病(AML)和一例骨髓細胞異常增生症(MDS)。2月23日,FDA發布公(gōng)告稱将藍鳥公(gōng)司治療SCD的LentiGlobin基因治療臨床試驗方案擱置。在經過FDA近一月的審查後,藍鳥生物(wù)宣布,其LentiGlobin基因療法是“極不可(kě)能(néng)(very unlikely)”導緻接受治療的鐮狀細胞病患者出現AML的,數據證明LentiGlobin基因療法并不會使患者出現異常綜合征,藍鳥生物(wù)現在正與FDA談判計劃恢複臨床試驗。
無獨有(yǒu)偶,在2020年8月時,FDA也拒絕過BioMarin的治療A型血友病的基因療法BMN270,因懷疑血友病患者接受基因治療不能(néng)終身受益,要求BioMarin提供所有(yǒu)研究參與者的兩年随訪安(ān)全性和有(yǒu)效性數據;此後,不到半年的時間,UniQure的一項針對B型血友病的基因療法也被美國(guó)FDA叫停,起因是一位志(zhì)願者患肝癌。針對這些問題,BioMarin 仍然希望其療法獲得批準;UniQure 認為(wèi)癌症病例不太可(kě)能(néng)與治療相關,臨床試驗也在繼續進行中(zhōng)。
這一次的烏龍事件也隻是讓大家虛驚一場,基因治療手段仍然被寄予厚望,Zynteglo的獲批是一個好的開始,國(guó)内外藥企對于血液疾病的基因治療持續布局,下一個上市的基因治療藥物(wù)能(néng)否花(huā)落血液疾病領域,也讓我們拭目以待。
1、基因療法用(yòng)于血友病
血友病(Hemophilia)是一種X染色體(tǐ)連鎖的隐性遺傳性出血性疾病,可(kě)分(fēn)為(wèi)血友病A(血友病甲,缺乏凝血因子Ⅷ,患病人數約占80%~85%)、血友病B(血友病乙,缺乏凝血因子Ⅸ,患病人數約占15%~20%)和血友病C(血友病丙,缺乏凝血因子Ⅺ,罕見)。患者因凝血因子基因缺陷導緻凝血功能(néng)障礙,終身具(jù)有(yǒu)輕微創傷後出血傾向,重症患者沒有(yǒu)明顯外傷也可(kě)發生“自發性”出血。血友病患者自出生時即可(kě)發病,伴随終身,如果得不到标準規範的治療,緻殘及緻死率很(hěn)高。
目前臨床上治療血友病常規方案是替代治療,即給患者補充所缺乏的凝血因子,但這種方案存在缺陷,如凝血因子在體(tǐ)内半衰期短,需反複注射等,不能(néng)治愈,需要終身治療,但仍有(yǒu)出血風險,這不僅影響患者的正常生活,且治療費用(yòng)昂貴,給患者帶來很(hěn)大的經濟負擔。已上市的凝血因子代表産(chǎn)品如:Baxalta的Advate/Recombinate,諾和諾德(dé)的Novoseven,拜耳公(gōng)司的KogenateFS等。Biogen的長(cháng)效凝血因子Alprolix和Eloctate、拜耳的重組長(cháng)效凝血因子 Kovaltry 也相繼獲批上市,長(cháng)效凝血因子藥物(wù)的市場和地位不斷拓展和鞏固。
近年來,市面上也出現了治療血友病的創新(xīn)藥,如羅氏的Hemlibraâ(Emicizumab,艾美賽珠單抗)是血友病藥物(wù)研發20年來首個獲得FDA批準的用(yòng)于治療A型血友病的新(xīn)藥。根據2019年羅氏财報,Hemlibra年銷售額達13.8億瑞士法郎,增長(cháng)超500%,Hemlibra需每周皮下注射一次,按照羅氏的定價,患者需要承擔第一年48.2萬美元、此後44.8萬美元/年的用(yòng)藥成本。
基因療法對血友病的治療提供了“一勞永逸”的新(xīn)思路,傳統藥物(wù)及像Hemlibra等新(xīn)型抗體(tǐ)藥物(wù)将直面基因療法的沖擊。早在1991年,我國(guó)科(kē)學(xué)家就進行了世界上首例血友病B的基因治療臨床試驗。現階段多(duō)個基因治療臨床試驗已經表現出了良好的療效與進展,如BioMarin公(gōng)司的A型血友病基因療法BMN 270已于近期提交了BLA申請,Sangamo/輝瑞的SB-525也處于III期臨床階段,血友病的用(yòng)藥市場格局即将被基因療法所改變。
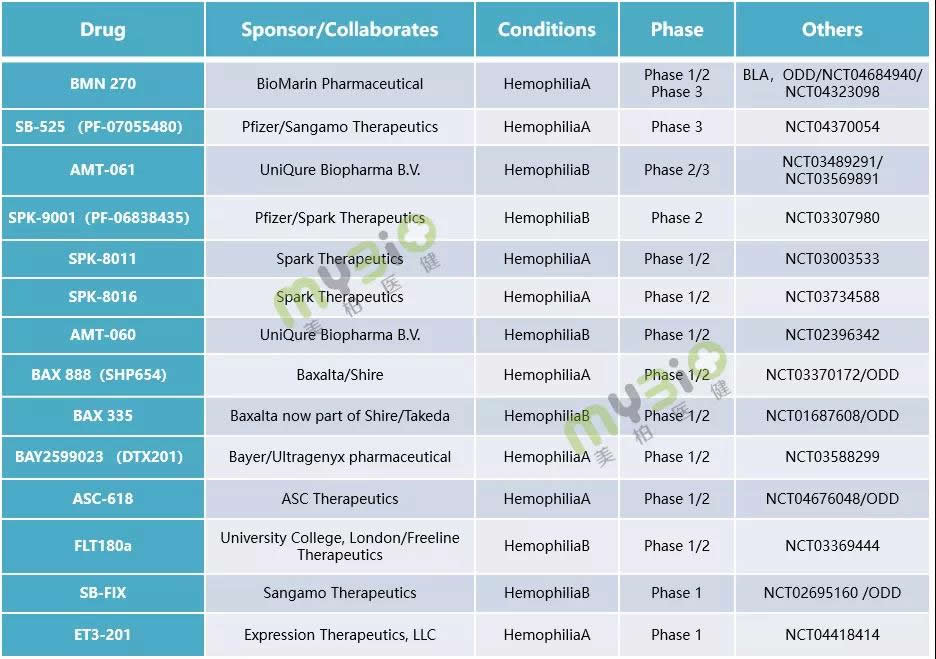
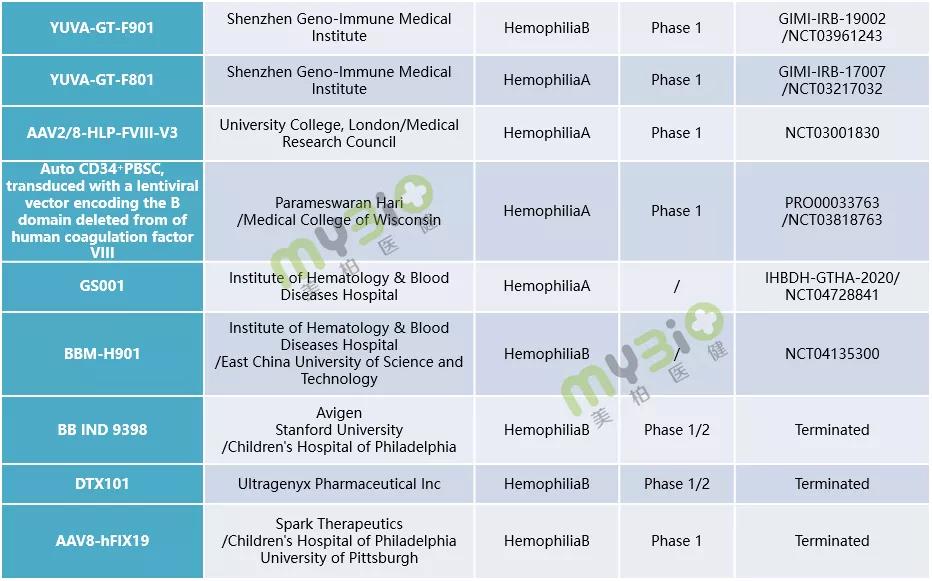
▲表1 處于臨床階段的部分(fēn)血友病基因治療候選療法
數據來源:https://www.clinicaltrials.gov
血友病基因治療的主要模式為(wèi)載體(tǐ)介導和細胞介導。載體(tǐ)介導即利用(yòng)載體(tǐ)将目的基因轉入靶細胞,使其在靶細胞中(zhōng)表達。細胞介導即提取患者細胞并利用(yòng)ZFN、TALEN或CRISPR/Cas9等基因編輯技(jì )術進行基因改造,擴增後移植入患者體(tǐ)内。基因治療可(kě)以使血友病患者體(tǐ)内自行表達FVIII或FIX,甚至可(kě)達正常水平,這使之成為(wèi)“一次性”治愈血友病的唯一手段。
研發基因療法用(yòng)于治療血友病的代表公(gōng)司:
(1)BioMarin
BioMarin創立于1996年,總部位于美國(guó),是一家針對慢性基因性疾病研發的公(gōng)司。
BioMarin的候選産(chǎn)品BMN 270正在進行3期臨床試驗,已經獲得美國(guó)FDA授予的孤兒藥和突破性療法認定,也已獲得而歐盟PRIME資格。其生物(wù)制品許可(kě)申請(BLA)已被FDA受理(lǐ),優先審核用(yòng)于治療嚴重A型血友病患者,這是美國(guó)第一個針對血友病的基因治療産(chǎn)品,也是有(yǒu)望成為(wèi)第一個被批準用(yòng)于治療A型血友病患者的基因療法。
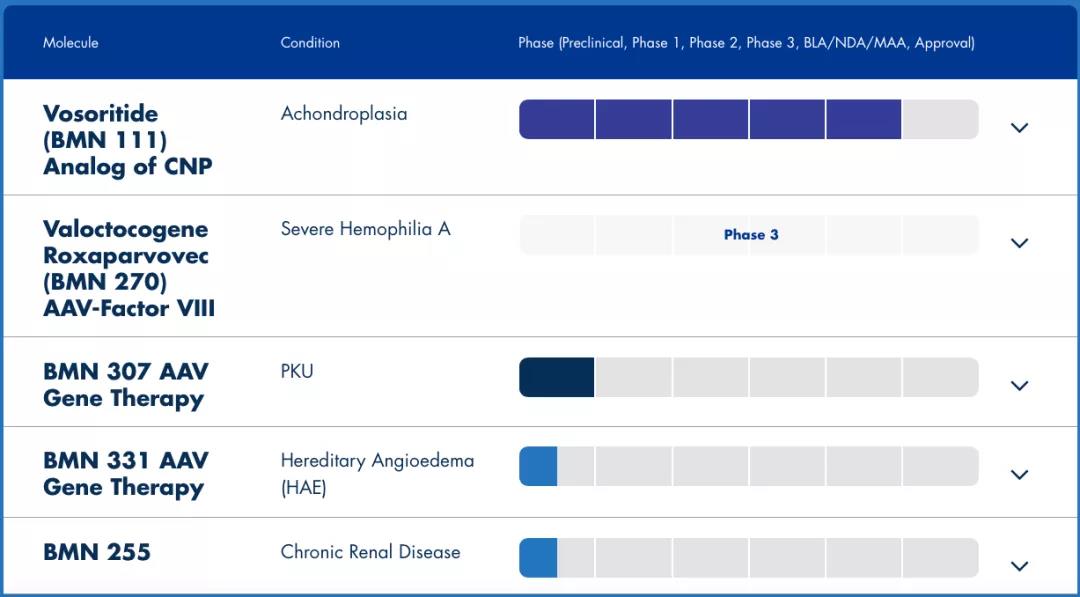
▲圖片來源:BioMarin官方網站
(2)Spark Therapeutics
Spark成立于2013年,總部位于賓夕法尼亞,是一家專注于遺傳疾病基因治療産(chǎn)品開發的公(gōng)司,2019年12月,羅氏以48億美金的價格完成對Spark的收購(gòu)。
Spark最初是研究罕見病特效孤兒藥的公(gōng)司,2017年年底,其針對罕見眼科(kē)疾病的基因療法Luxturna獲FDA批準,成為(wèi)首個在美國(guó)上市的基因療法。其兩款治療血友病的明星産(chǎn)品SPK-9001和SPK-8011在臨床上也表現出很(hěn)好的療效,此外,另一款基于AAV載體(tǐ)表達凝血因子VIII的基因療法SPK-8016也處于臨床階段。
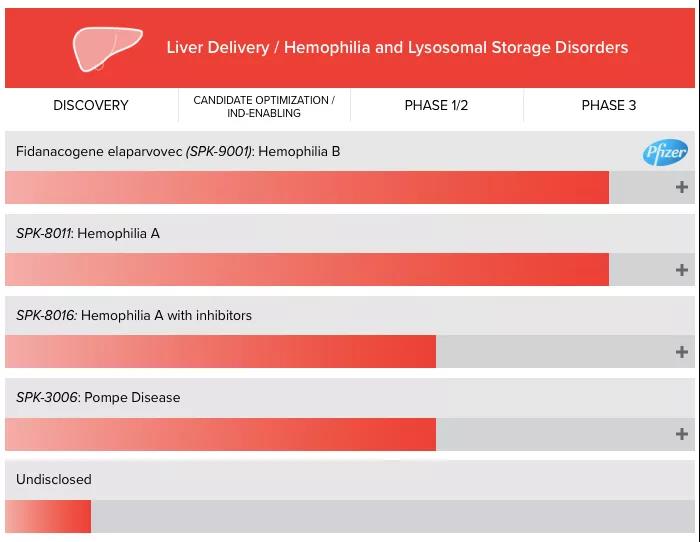
▲圖片來源:Spark官方網站
(3)UniQure
UniQure創立于1998年,總部位于荷蘭,是一家從事基因治療藥物(wù)開發的生物(wù)制藥公(gōng)司。UniQure擁有(yǒu)歐洲上市的首個基因療法Glybera,用(yòng)于治療脂蛋白脂酶缺乏症(LPLD)。
2020年6月,UniQure宣布與CSL Behring簽訂許可(kě)協議, CSLBehring獲得UniQure在B型血友病适應症上的的基因治療産(chǎn)品AMT-061的全球獨家權利,總交易額超20億美元。
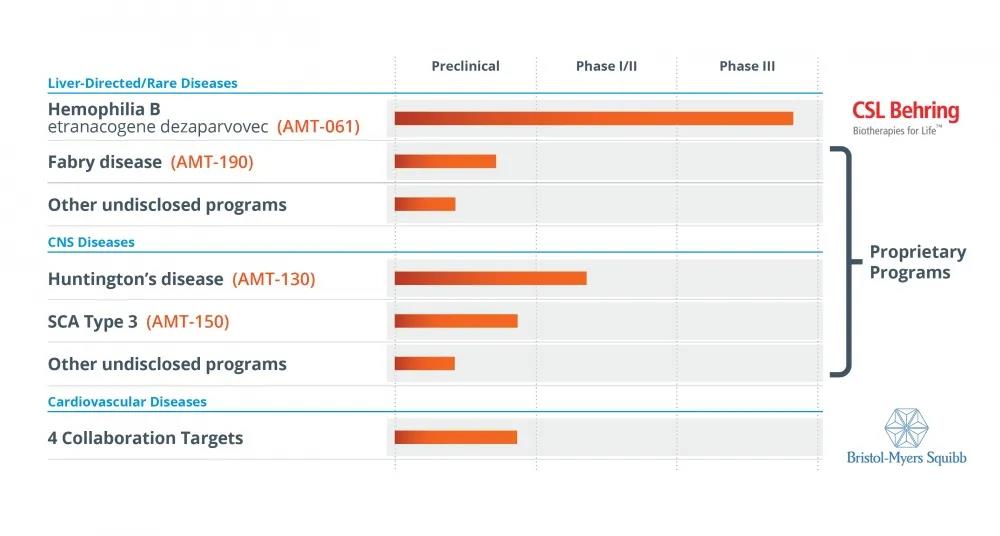
▲圖片來源:UniQure官方網站
(4)Sangamo Therapeutics
Sangamo創立于1995年,總部位于美國(guó),是一家專注于基因編輯、基因治療和細胞治療平台技(jì )術的生物(wù)制藥公(gōng)司。Sangamo在ZFN基因編輯技(jì )術上深耕20餘年,ZFN技(jì )術相關的專利基本由該公(gōng)司持有(yǒu),獲得包括鋅指蛋白設計、篩選、優化、實驗室及臨床應用(yòng)等多(duō)項專利。
2017年5月,Sangamo與Pfizer就一款A型血友病基因療法SB-525,簽署了全球獨家合作(zuò)和許可(kě)協議,交易金額達5.45億美元。目前,FDA已授予SB-525孤兒藥地位和快速通道認定。此外,2018年12月,Sangamo宣布1/2期臨床試驗評估SB-FIX的第一位患者進行治療,這是全球首個利用(yòng)鋅指核酸酶(ZFN)技(jì )術并且針對B型血友病的在體(tǐ)基因編輯臨床試驗,且該療法在2016年便獲FDA授予的孤兒藥資格。
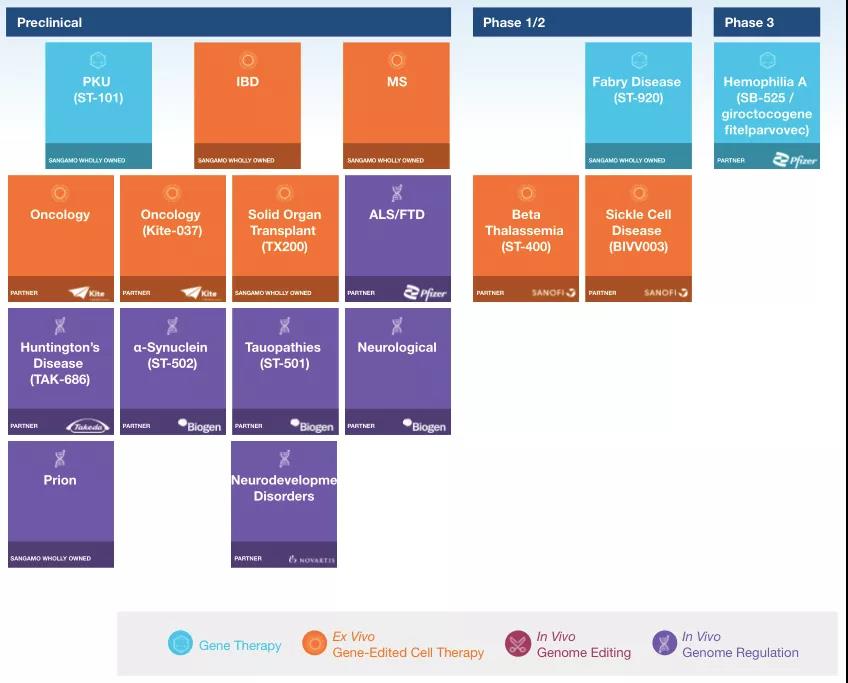
▲圖片來源:Sangamo官方網站
(5)ASC Therapeutics
ASC Therapeutics是一家快速發展的生物(wù)技(jì )術公(gōng)司,通過其專有(yǒu)的基因編輯平台TARGATTTM和其他(tā)基因編輯技(jì )術開發治療型産(chǎn)品,為(wèi)尚珹投資在醫(yī)療領域的投資項目之一。
目前研發管線(xiàn)包括幾個臨床前階段的項目,重點關注血液病的研究。根據clinicaltrials.gov顯示,2021年4月,ASC Therapeutics公(gōng)司将開展ASC-618治療中(zhōng)重度血友病A的安(ān)全性及初步療效評價臨床研究。另外,管線(xiàn)上還有(yǒu)治療A型血友病的基因療法ASC-518、治療B型血友病的基因療法ASC-519及治療β 地中(zhōng)海貧血的基因療法ASC-520處于早期研究階段。
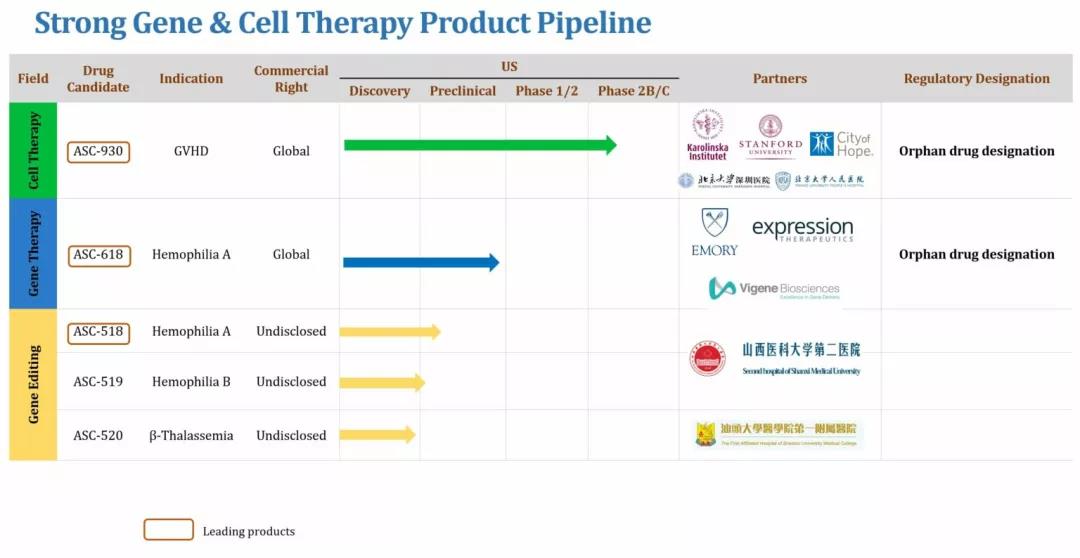
▲圖片來源:ASC Therapeutics官方網站
(6)Freeline Therapeutics
Freeline創立于2015年,主要專注于利用(yòng)基因療法的潛力為(wèi)患有(yǒu)慢性全身性疾病的病人提供治愈性治療方法。Freeline開發了一種改進的AAV病毒衣殼,這種強大的衣殼在B型血友病患者的臨床試驗中(zhōng)得到驗證。

2018年,Freeline完成1.16億美元(約合人民(mín)币7.54億元)的B輪融資,以推動其主打産(chǎn)品用(yòng)于治療B型血友病和法布裏病的臨床開發,以及其他(tā)産(chǎn)品管線(xiàn)的進展。同時新(xīn)融資也将幫助Freeline進一步提高其基于AAV(腺相關病毒)衣殼的生産(chǎn)和進一步優化能(néng)力。

▲圖片來源:Freeline官方網站
(7)Ultragenyx Pharmacetical
Ultragenyx成立于2010年,總部位于加利福尼亞,是一家專注罕見病新(xīn)藥的研發和商(shāng)業化的生物(wù)醫(yī)藥公(gōng)司。
Ultragenyx與拜耳合作(zuò)開發的用(yòng)于治療A型血友病的基因療法BAY2599023 (DTX201)使用(yòng)的是Regenxbio專有(yǒu)的NAV AAVhu37載體(tǐ)。DTX201最初是由Dimension研發,Ultragenyx于2017年11月完成對Dimension Therapeutics的收購(gòu),獲得該産(chǎn)品。根據clinicaltrials.gov顯示,拜耳于2018年11月啓動BAY2599023(DTX201)關于成人嚴重血友病A的臨床試驗研究,這也是Bayer産(chǎn)品管線(xiàn)中(zhōng)唯一一款處于臨床階段的治療血友病的基因療法。
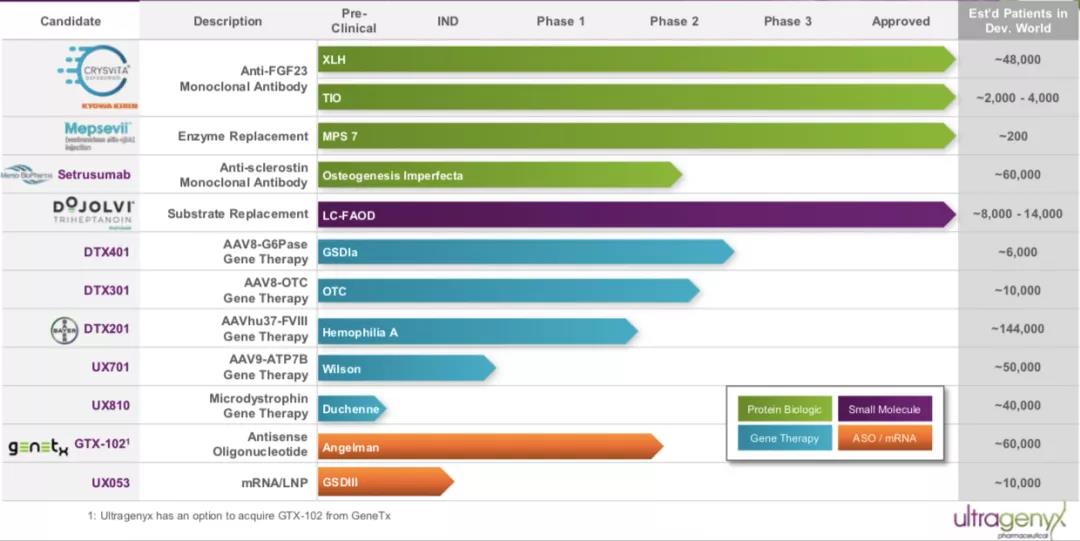
▲圖片來源:Ultragenyx官方網站
另外值得一提的是基因治療領域的新(xīn)秀Regenxbio,Regenxbio緻力于AAV(Adeno-associated virus,重組腺相關病毒)基因療法的開發和商(shāng)業化。Regenxbio擁有(yǒu)的NAV技(jì )術平台是一種專有(yǒu)的AAV基因遞送平台,包括100多(duō)種新(xīn)型AAV載體(tǐ),比如AAV7、AAV8、AAV9和AAVrh10。

目前,Regenxbio已将NAV技(jì )術許可(kě)給10餘家公(gōng)司,并據此開發了超20個候選産(chǎn)品,主要用(yòng)于治療神經退行性疾病、血液疾病、視網膜疾病等适應症,合作(zuò)方包括Novartis、Prevail、Pfizer、Takeda等企業。其中(zhōng)有(yǒu)2款治療A型血友病的基因候選産(chǎn)品,目前分(fēn)别由Takeda和Ultragenyx/Bayer進行後續開發。
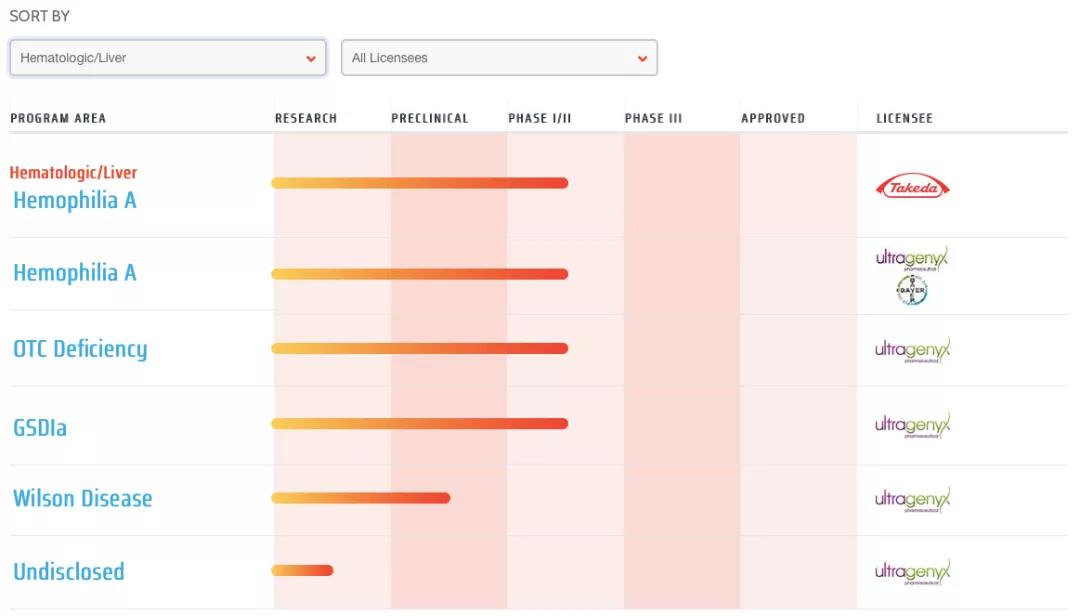
▲圖片來源:Regenxbio官方網站
(8)Generation Bio
Generation Bio創立于2016年,總部位于美國(guó),是一家創新(xīn)型基因藥物(wù)公(gōng)司,利用(yòng)特有(yǒu)的非病毒基因治療平台創建了一類新(xīn)型的基因治療産(chǎn)品。其創新(xīn)點在遞送系統,核心技(jì )術被稱為(wèi)non-viral closed-ended DNA(ceDNA),通過脂質(zhì)納米顆粒進入人體(tǐ),這項技(jì )術能(néng)避開基于病毒的基因治療中(zhōng)典型的免疫反應。Generation Bio自2018年來,先後完成三輪融資,并于2020年5月進行了IPO,同年6月于納斯達克上市。
Generation Bio的産(chǎn)品線(xiàn)包括針對肝髒和視網膜的罕見病和流行疾病的八個項目,其中(zhōng)苯丙酮尿症(PKU)和A型血友病進展最快,處于臨床前研究階段。
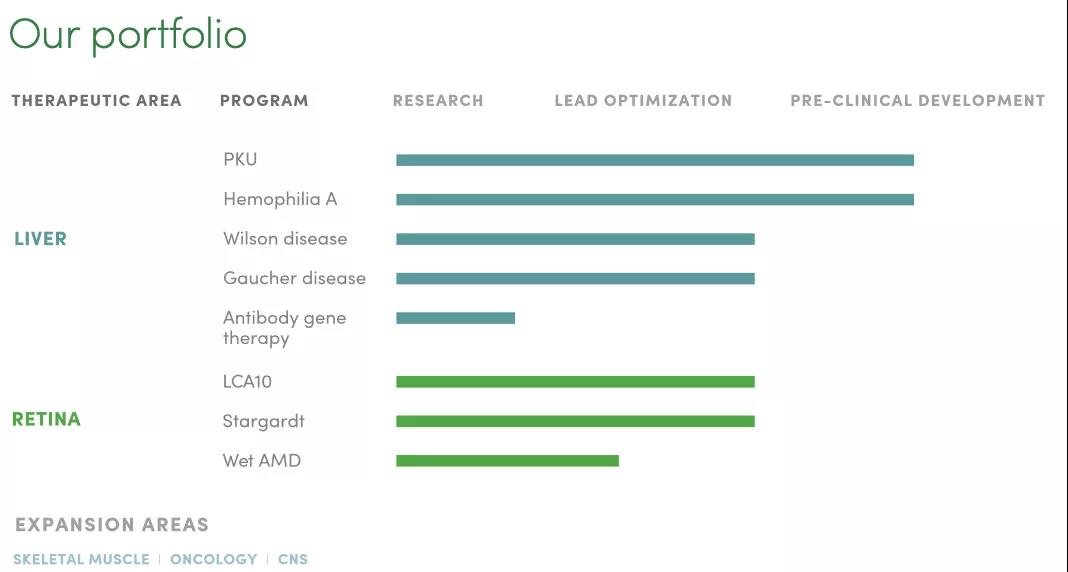
▲圖片來源:Generation Bio官方網站
(9)深圳市免疫基因治療研究院
深圳市免疫基因治療研究院是經深圳市人民(mín)政府批準設立的具(jù)有(yǒu)獨立法人資格的二類事業單位。研究院主要研究方向是針對癌症的CAR-T免疫細胞治療及針對基因相關疾病的治療。
深圳市免疫基因治療研究院采用(yòng)雙重幹細胞基因療法治療多(duō)項遺傳疾病,對七種基因疾病進行深入研究,包括異染性腦白質(zhì)營養不良、腎上腺腦白質(zhì)營養不良、地中(zhōng)海貧血、血友病、視網膜眼睛疾病、X連鎖嚴重聯合免疫缺陷和範可(kě)尼貧血。
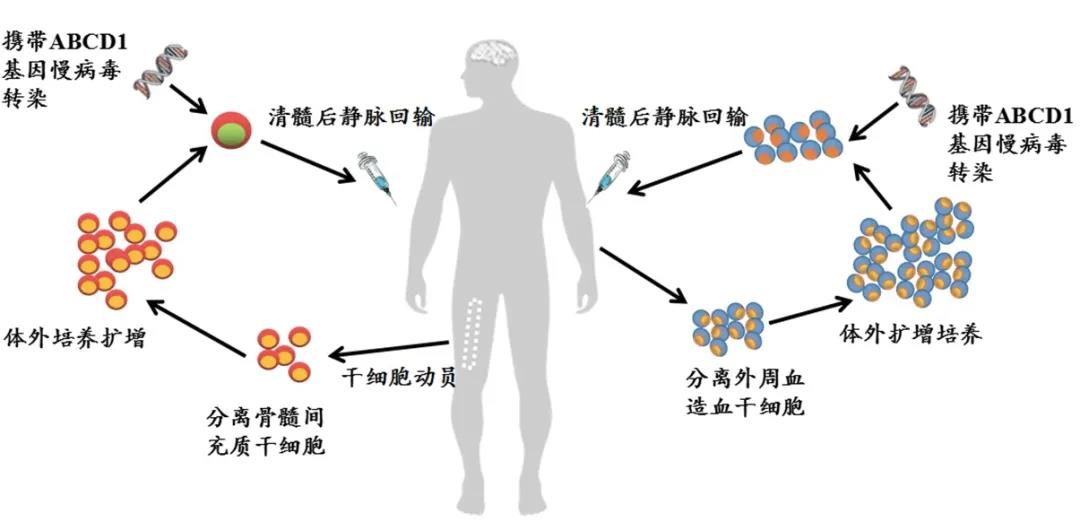
▲圖1 深圳市免疫基因治療研究院拟采用(yòng)的雙重幹細胞基因治療示意圖
圖片來源:深圳市免疫基因治療研究院官方網站
雖然,我國(guó)在1991年就開展了首個針對血友病的基因治療臨床試驗,但是直到近幾年才有(yǒu)血友病基因療法進一步開展臨床階段。中(zhōng)國(guó)醫(yī)學(xué)科(kē)學(xué)院血液學(xué)研究所&血液病醫(yī)院與華東理(lǐ)工(gōng)大學(xué)共同申請的靜脈輸注基于AAV的基因療法BBM-H901用(yòng)于治療血友病B臨床試驗(NCT04135300)于2019年10月發起,這也是國(guó)内首個AAV基因治療臨床試驗。
深圳市免疫基因治療研究院的YUVA-GT-F801、YUVA-GT-F901分(fēn)别用(yòng)于治療A型血友病與B型血友病,目前也處于1期臨床試驗階段。
此外,深圳市免疫基因治療研究院還有(yǒu)關于地中(zhōng)海貧血、範可(kě)尼貧血的基因治療試驗也正開展臨床。
(10)北京五加和基因科(kē)技(jì )有(yǒu)限公(gōng)司
五加和基因成立于2005年,技(jì )術團隊從事病毒載體(tǐ)系統研究20餘年,公(gōng)司緻力于為(wèi)pre-IND和IND階段基因藥物(wù)提供符合GMP标準的病毒載體(tǐ)制品研發生産(chǎn)服務(wù)。

公(gōng)司董事長(cháng)兼總經理(lǐ)董小(xiǎo)岩博士在2000年建立本元正陽基因技(jì )術股份有(yǒu)限公(gōng)司基因治療新(xīn)藥研發平台。2003年,其自主研發使用(yòng)AAV載體(tǐ)的血友病B基因藥物(wù)研發項目AAV2-hFIX獲批,系中(zhōng)國(guó)首個被批準的血友病B基因治療藥物(wù)臨床方案。2005年創建北京五加和,帶領團隊研發用(yòng)于治療B型血友病、A型血友病、SMA、DMD、ALS、遺傳性高脂血症、青光眼等26種疾病的基因藥物(wù)。
(11)四川至善唯新(xīn)生物(wù)科(kē)技(jì )有(yǒu)限公(gōng)司
至善唯新(xīn)成立于2018年,是一家專注rAAV基因藥物(wù)研發與颠覆式生産(chǎn)的國(guó)内基因治療領軍企業。公(gōng)司擁有(yǒu)基因療法領域的專業團隊,創始人董飚從事rAAV病毒載體(tǐ)研究超過十年,在基因療法藥物(wù)設計與規模化生産(chǎn)方面均取得了突破性進展,治療領域涵蓋血液疾病、罕見病等多(duō)個疾病領域。
至善唯新(xīn)擁有(yǒu)全球領先的新(xīn)型rAAV生産(chǎn)系統,針對A型血友病和B型血友病都有(yǒu)了相應的rAAV基因藥物(wù)臨床管線(xiàn)布局,已經完成臨床前的動物(wù)模型驗證。其中(zhōng),針對B型血友病的臨床管線(xiàn)是公(gōng)司眼下重點推進的項目,利用(yòng)有(yǒu)自主專利的規模化載體(tǐ)生産(chǎn)技(jì )術和高效IX因子,開發治療B型血友病的rAAV藥物(wù),該項目将于2021年提交臨床批件注冊申報。除布局血友病方向的管線(xiàn)外,至善唯新(xīn)利用(yòng)自身在于rAAV基因治療領域儲備的技(jì )術優勢,在抗衰老和神經退行性疾病方向也有(yǒu)相應的管線(xiàn)布局,包括針對帕金森症、老年癡呆症的rAAV基因藥物(wù)研究等。
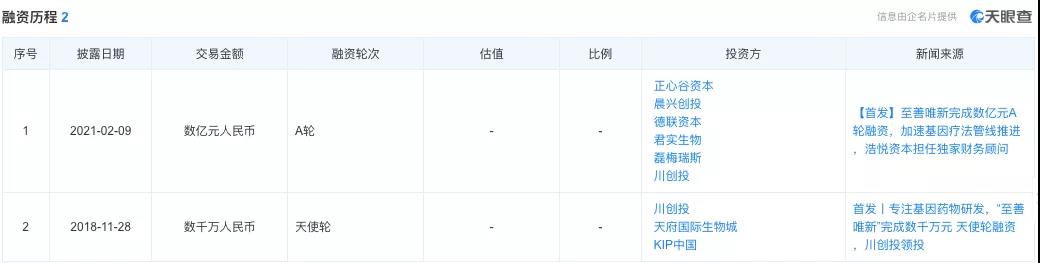
▲圖片來源:天眼查官方網站
至善唯新(xīn)成立不足半年,便獲得由川創投領投的數千萬人民(mín)币天使輪融資;2021年2月,又(yòu)完成了數億元人民(mín)币的A輪融資,用(yòng)來加速基因療法管線(xiàn)的推進,其中(zhōng),君實生物(wù)持有(yǒu)至善唯新(xīn)約6.6%的股權。
(12)信念醫(yī)藥科(kē)技(jì )(蘇州)有(yǒu)限公(gōng)司
信念醫(yī)藥成立于2018年,緻力于基因治療藥物(wù)的産(chǎn)業化研發和臨床應用(yòng),包括腺相關病毒基因治療載體(tǐ)的前端篩選、生産(chǎn)工(gōng)藝優化、GMP生産(chǎn)、臨床質(zhì)控标準和臨床試驗等。信念醫(yī)藥計劃從生物(wù)科(kē)技(jì )公(gōng)司逐步轉型為(wèi)生物(wù)醫(yī)藥公(gōng)司,目前已完成數千萬的天使輪與數億元的 A 輪融資。
信念的産(chǎn)品布局主要專注在開發以AAV為(wèi)載體(tǐ)的基因療法,産(chǎn)品線(xiàn)包括血友病 A、血友病 B、帕金森症、老年黃斑變性、粘多(duō)糖貯積症、肌萎縮側索硬化症、遺傳性血管水腫、嗜血細胞綜合征、法布裏疾病等适應症,其中(zhōng)研發最快的兩個産(chǎn)品就是血友病B和血友病A。
華東理(lǐ)工(gōng)大學(xué)與血液所申報的血友病基因治療産(chǎn)品BBM-H901正是出自信念醫(yī)藥的子公(gōng)司上海信緻醫(yī)藥科(kē)技(jì )有(yǒu)限公(gōng)司臨床藥物(wù)生産(chǎn)場地,位于華東理(lǐ)工(gōng)大學(xué)國(guó)家大學(xué)科(kē)技(jì )園梅隴基地内。
此外,國(guó)際上還有(yǒu)很(hěn)多(duō)公(gōng)司正在積極布局血友病基因治療産(chǎn)品,如諾和諾德(dé)與藍鳥生物(wù)于2019年10月達成合作(zuò)協議,雙方合作(zuò)重點利用(yòng)藍鳥生物(wù)的megaTAL技(jì )術開發A型血友病的基因療法;再生元與Intellia Therapeutics擴大雙方自2016年的合作(zuò),交易額達1億美元,雙方合作(zuò)重點是開發治療A型血友病和B型血友病的潛在CRISPR / Cas9編輯基因治療候選藥物(wù);賽諾菲與合作(zuò)已久的慢病毒載體(tǐ)開發商(shāng)Oxford BioMedica(OXB)利用(yòng)其開發和生産(chǎn)用(yòng)于治療血友病的慢病毒載體(tǐ),首次開發基于慢病毒的體(tǐ)内給藥血友病基因療法等。
2、基因療法用(yòng)于β地中(zhōng)海貧血
地中(zhōng)海貧血(Thalassemia,地貧)即珠蛋白生成障礙性貧血,是一組常染色體(tǐ)遺傳的溶血性貧血疾病,其緻病機制是珠蛋白基因缺陷使血紅蛋白中(zhōng)的珠蛋白肽鏈有(yǒu)一種或幾種合成減少或不能(néng)合成,導緻血紅蛋白的組成成分(fēn)改變,進而引發紅細胞壽命縮短,表現為(wèi)慢性溶血性貧血。根據珠蛋白鏈缺乏種類不同,地中(zhōng)海貧血分(fēn)為(wèi)α型、β型、δβ型、δ型和ebgδ型,其中(zhōng)臨床上以β和α型地貧最為(wèi)常見,α-地貧又(yòu)分(fēn)靜止型、輕型、中(zhōng)間性和重型;β-地貧又(yòu)分(fēn)輕型、中(zhōng)間型和重型。
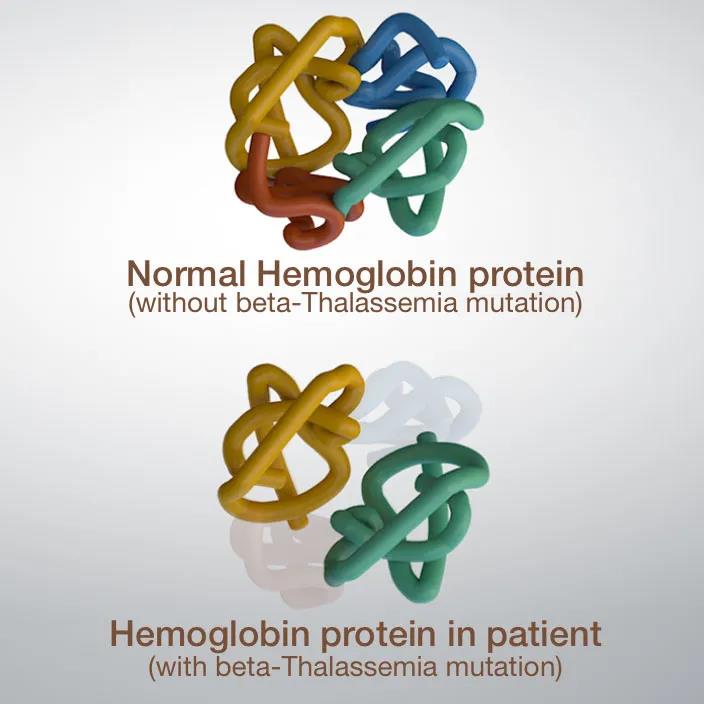
▲圖2 β-地貧緻病機制示意圖
圖片來源:Learn. Genetics,Gene TherapySuccesses
目前,針對β-地貧的療法有(yǒu)輸血替代治療、脾髒切除和造血幹細胞移植治療等。其中(zhōng)定期輸血是臨床上比較常規的治療方案,患者需要終身治療,治療費用(yòng)昂貴且易産(chǎn)生輸血副反應,還須同時接受去鐵治療,但去鐵治療也同樣會伴随嚴重不良反應,常用(yòng)鐵螯合劑包括得斯芬、奧貝安(ān)可(kě)、恩瑞格等;對于經正常輸血治療及去鐵治療後鐵負荷仍增加的患者考慮脾髒切除,但此治療方案會增加嚴重敗血症發生的風險,且對重症β-地貧患者效果仍差強人意;造血幹細胞移植治療是目前能(néng)夠根治的唯一方案,可(kě)通過骨髓移植、外周血幹細胞移植、臍血移植等方案将健康人的造血幹細胞移植至病人體(tǐ)内,但配型十分(fēn)困難,且供體(tǐ)來源有(yǒu)限,即使配型成功仍需長(cháng)期服用(yòng)免疫抑制藥物(wù),治療費用(yòng)也十分(fēn)昂貴。
在β 地中(zhōng)海貧血(TDT)治療領域,也有(yǒu)一些新(xīn)藥獲批,BMS的Reblozyl就是第一個獲FDA批準治療β 地中(zhōng)海貧血相關貧血的藥物(wù),同時也是十多(duō)年來第一個獲FDA批準用(yòng)于需要輸注紅細胞(RBC)且接受一種紅細胞生成刺激劑治療失敗的骨髓增生異常綜合症(MDS)患者的新(xīn)治療方案。特别值得注意的是,在需要立即糾正貧血的患者中(zhōng),Reblozyl不适用(yòng)于作(zuò)為(wèi)紅細胞輸注的替代品。此前,華爾街(jiē)投行Jefferies分(fēn)析師預測,Reblozyl獲FDA批準後的年銷售峰值将達到20億美元。
基因療法為(wèi)β地中(zhōng)海貧血提供了新(xīn)的治療思路,将造血幹細胞從病人自身的外周血中(zhōng)收集後,通過病毒載體(tǐ)導入正常的珠蛋白基因以使細胞功能(néng)恢複正常,再将改造後的造血幹細胞回輸給病人。這種治療方案的優勢在于,供體(tǐ)來源不需要通過捐贈、異體(tǐ)移植,解決了幹細胞來源不足以及配型困難等問題,一次治療就可(kě)能(néng)滿足永久性的“治愈”,有(yǒu)望取代目前并不完美的治療方案。
2019年5月,全球首個治療輸血依賴型β地中(zhōng)海貧血的基因療法Zynteglo獲得歐洲藥品管理(lǐ)局(EMA)有(yǒu)條件批準,也有(yǒu)多(duō)家企業正在進行β 地中(zhōng)海貧血基因療法的臨床及臨床前的實驗研究。
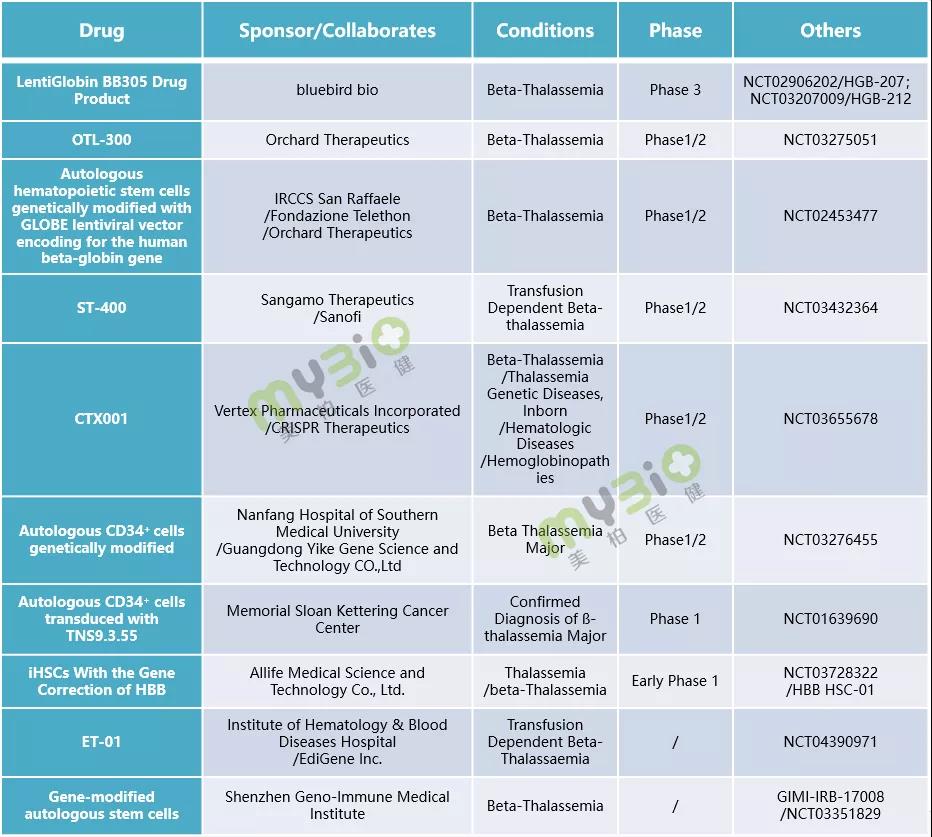
▲表2 處于臨床階段的部分(fēn)β 地中(zhōng)海貧血基因治療候選療法
數據來源:https://www.clinicaltrials.gov
這種一次性的基因治療方法,可(kě)直接解決β地中(zhōng)海貧血的内在基因病因,有(yǒu)潛力使患者擺脫輸血依賴(輸血非依賴),一旦成功,患者将終身受益。
研發基因療法用(yòng)于治療β地中(zhōng)海貧血的代表公(gōng)司:
(1)bluebird bio
藍鳥生物(wù)公(gōng)司(bluebird bio)創立于1992年,總部位于美國(guó),原名(míng)Genetix Pharmaceuticals, Inc.,于2010年9月改為(wèi)bluebird bio,是一家緻力于為(wèi)治療嚴重的遺傳疾病和罕見疾病開發革命性基因療法的臨床階段生物(wù)技(jì )術公(gōng)司。

藍鳥生物(wù)的基因産(chǎn)品LentiGlobin治療β 地中(zhōng)海貧血已獲EMA批準,這是針對β-地中(zhōng)海貧血的首款基因療法,LentiGlobi
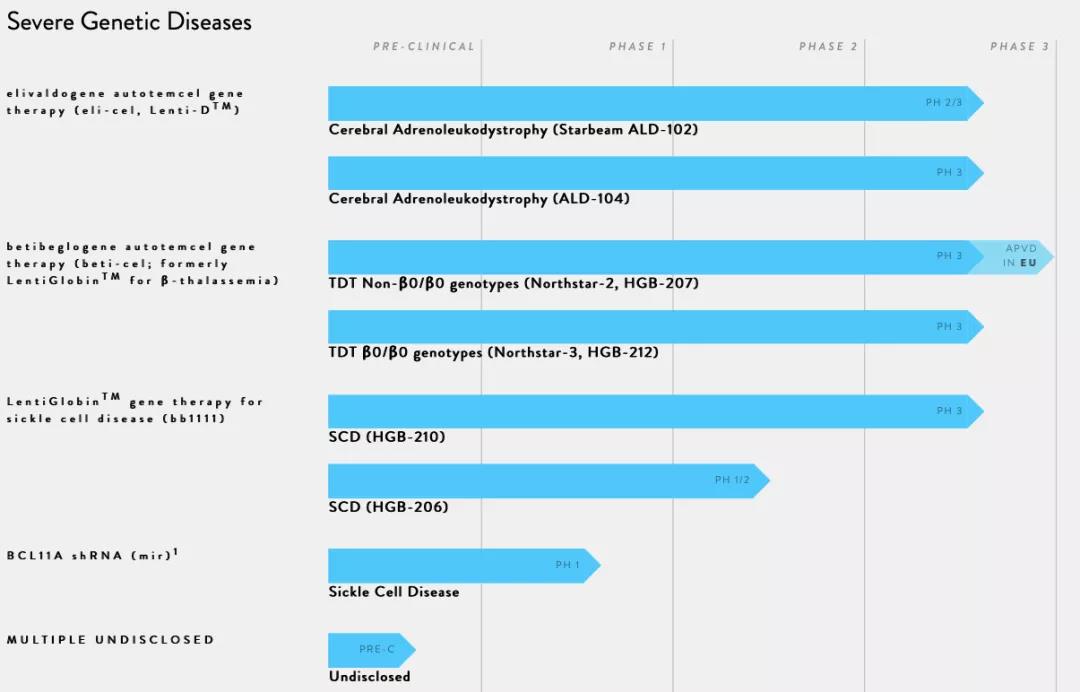
n的另一适應症SCD正處于臨床研究階段。
▲圖片來源:bluebird bio官方網站
(2)Orchard Therapeutics
Orchard成立于2015年,位于英國(guó),是一家緻力于為(wèi)患有(yǒu)嚴重和危及生命的孤兒疾病的患者提供變革性基因治療的公(gōng)司,将利用(yòng)離體(tǐ)自體(tǐ)造血幹細胞基因治療的潛力來恢複正常的基因功能(néng)。

OTL-300是一種實驗性自體(tǐ)體(tǐ)外慢病毒基因療法,2018年4月,Orchard從葛蘭素史克收購(gòu)該基因療法,EMA已授予OTL-300治療TDT的優先藥物(wù)資格。繼收購(gòu)GSK基因療法後,Orchard獲1.5億美元C輪融資,随後IPO上市。
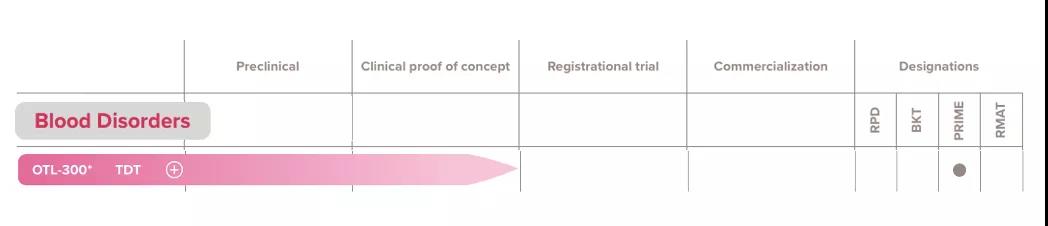
▲圖片來源:Orchard官方網站
(3)CRISPR Therapeutics/Vertex
CRISPR Therapeutics于2013年10月成立于瑞士,研究中(zhōng)心在馬薩諸塞州劍橋,由獲得2020年諾貝爾化學(xué)獎的Emmanuelle Charpentier及其同事創立,緻力于利用(yòng)其專利 CRISPR/Cas9 基因編輯平台開發革命性藥物(wù)。Vertex成立于1989年,是一家緻力于開發治療嚴重疾病藥物(wù)的生物(wù)技(jì )術公(gōng)司,囊性纖維化治療領域的全球領導者,目前已上市多(duō)款囊性纖維化療法。CRISPR Therapeutics與Vertex也建立了戰略合作(zuò)夥伴關系,開發基于CRISPR技(jì )術的基因治療方案。

2015年,CRISPR與Vertex達成合作(zuò),雙方協議利用(yòng)CRISPR/Cas9 基因編輯技(jì )術去發現和開發針對人類疾病内在基因原因的潛在新(xīn)療法,CTX001就是利用(yòng)這項合作(zuò)的首個成果。2018年,CTX001獲得了美國(guó)和歐洲監管機構的新(xīn)藥研究申請批件,這也是全球首個由制藥公(gōng)司發起的體(tǐ)外CRISPR療法的新(xīn)藥臨床試驗。目前,CTX001處于I/II期臨床試驗階段,獲得了FDA 授予的再生醫(yī)學(xué)高級療法(RMAT)、快速審評通道、孤兒藥和罕見兒科(kē)疾病藥物(wù)稱号,還獲得EMA授予的針對鐮狀細胞病和 β 地中(zhōng)海貧血的孤兒藥稱号以及針對鐮狀細胞病的優先審評藥物(wù)資格。

▲圖片來源:CRISPR官方網站
(4)Editas Medicine
由CRISPR領域的領軍人物(wù)張鋒和Jennifer Doudna共同創建的Editas成立于2013年,是最早上市的CRISPR-Cas9技(jì )術公(gōng)司。
公(gōng)司的研發管線(xiàn)中(zhōng)治療伯氏先天性黑蒙症的EDIT-101

療法進展最快,已經進入臨床階段,其次是EDIT-301療法,用(yòng)于鐮狀細胞病與β 地中(zhōng)海貧血。
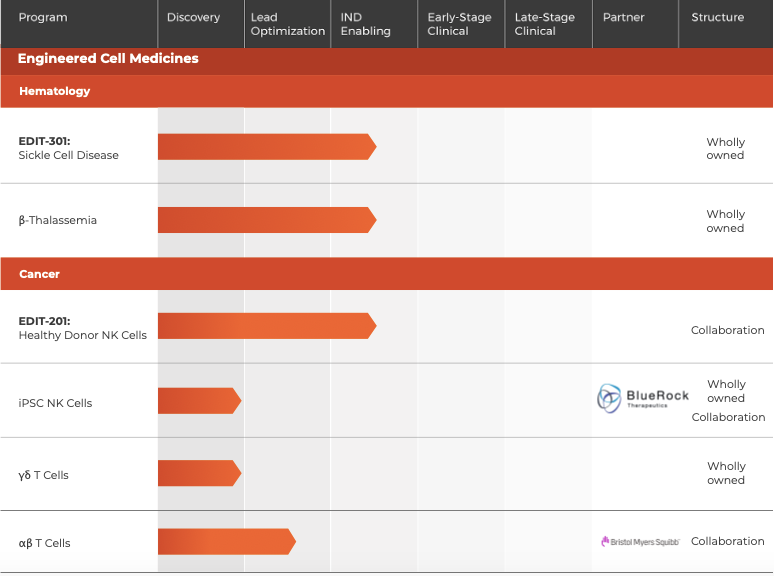
▲圖片來源:Editas官方網站
(5)Sangamo Therapeutics/Sanofi
上文(wén)提到,Sangamo與Pfizer合作(zuò)開發A型血友病基因療法SB-525,Sangamo還與Sanofi合作(zuò)将ZFN基因編輯技(jì )術應用(yòng)于輸血依賴性β-地中(zhōng)海貧血的治療,其相關産(chǎn)品ST-400處于1/2期臨床試驗階段。
近年來,Sanofi不斷布局基因療法領域。自2018年1月完成收購(gòu)專注于血友病的Bioverativ公(gōng)司後,Sanofi也公(gōng)布了許多(duō)基因療法相關的積極消息,除與Sangamo合作(zuò)開發ST-400外,雙方還共同研究治療鐮狀細胞病的基因療法BIVV003;2019年,Sanofi首個基于AAV的基因療法進入臨床,用(yòng)于治療由常染色體(tǐ)隐性鳥苷酸環化酶2D(GUCY2D)突變引起的Leber先天性黑朦(LCA)的罕見眼科(kē)疾病;2021年2月,Sanofi與Sirion也達成合作(zuò),雙方共同開發基于病毒載體(tǐ)的基因傳遞技(jì )術。
(6)博雅輯因(北京)生物(wù)科(kē)技(jì )有(yǒu)限公(gōng)司
博雅輯因成立于2015年,是一家緻力于通過國(guó)際前沿的基因組編輯技(jì )術,為(wèi)多(duō)種遺傳疾病和癌症加速藥物(wù)研究以及開發創新(xīn)療法的生物(wù)醫(yī)藥企業。博雅輯因有(yǒu)造血幹細胞平台、通用(yòng)型CAR-T平台、體(tǐ)内療法-RNA堿基編輯平台、高通量基因組編輯篩選-新(xīn)藥研發平台四大平台。其中(zhōng),造血幹細胞平台通過基因編輯自體(tǐ)造血幹細胞,針對β地中(zhōng)海貧血病和其他(tā)貧血病的創新(xīn)療法。

博雅輯因利用(yòng)四大技(jì )術平台已經開發了十餘條産(chǎn)品管線(xiàn),其中(zhōng)進展最快的是一種體(tǐ)外基因療法,針對輸血依賴型β地中(zhōng)海貧血的ET-01和針對癌症的異體(tǐ)CAR-T ET-02。ET-01基于CRISPR的基因編輯療法,通過提高患者胎兒血紅蛋白水平彌補正常β血紅蛋白的不足。臨床前研究證明了該方法的可(kě)行性。2020年10月,中(zhōng)國(guó)國(guó)家藥品監督管理(lǐ)局受理(lǐ)了我國(guó)首個CRISPR基因編輯療法臨床試驗申請。
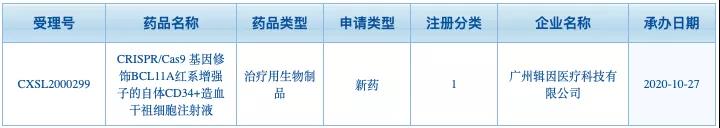
▲圖片來自:國(guó)家藥品監督管理(lǐ)局藥品審評中(zhōng)心官網
博雅輯因的ET-01項目也受到國(guó)際上的認可(kě),2019年,在第61屆美國(guó)血液學(xué)年會(ASH)上,博雅輯因發布了其β地中(zhōng)海貧血基因編輯治療項目的規模化生産(chǎn)及臨床前安(ān)全性和有(yǒu)效性試驗數據。
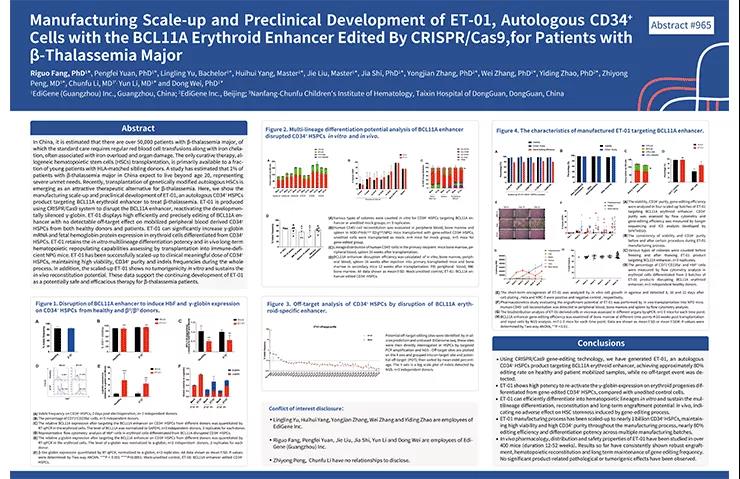
▲圖片來自:博雅輯因官方網站
(7)北京呈諾醫(yī)學(xué)科(kē)技(jì )有(yǒu)限公(gōng)司
呈諾醫(yī)學(xué)(Allife Medical Science and Technology Co., Ltd.)創立于2017年,由中(zhōng)英兩國(guó)科(kē)學(xué)家創辦(bàn)。公(gōng)司立足于自主研發的iPSC誘導多(duō)能(néng)幹細胞技(jì )術平台,緻力于開發國(guó)際前沿的創新(xīn)型功能(néng)細胞治療藥物(wù)。

呈諾醫(yī)學(xué)擁有(yǒu)成熟的誘導多(duō)能(néng)幹細胞(iPSC)制備技(jì )術,以此為(wèi)基礎研發了針對罕見病、帕金森、糖尿病和心血管疾病的治療産(chǎn)品,現階段将側重于法布雷(Fabry)和漸凍症(ALS),這兩種罕見病在中(zhōng)國(guó)有(yǒu)十幾萬患者需要治療。另外,呈諾醫(yī)學(xué)的腫瘤免疫細胞産(chǎn)品以自然殺傷細胞(NK)為(wèi)基礎,從技(jì )術角度看,CAR-NK療法安(ān)全性更好,且易獲得,易操控,免疫原性較低;從臨床結果看, CAR-NK對癌細胞的殺傷效果同CAR-T療法也不相上下。
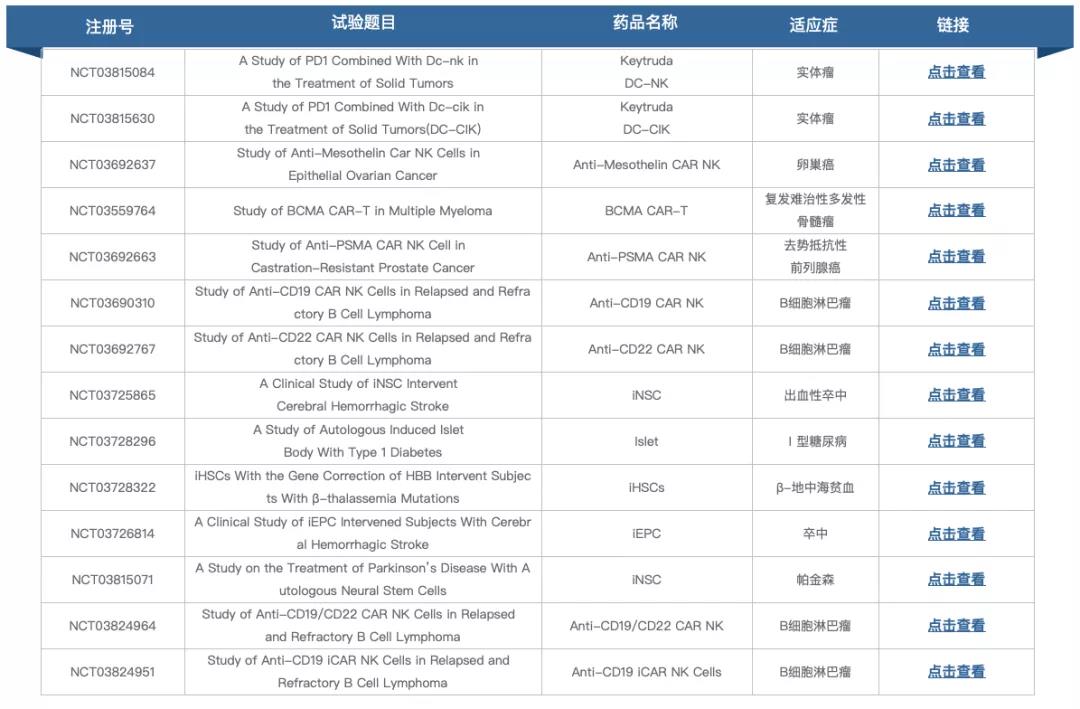
▲圖片來源:呈諾醫(yī)學(xué)官方網站
跟據clinicaltrials.gov顯示,呈諾醫(yī)學(xué)CRISPR-Cas9處理(lǐ)的誘導造血幹細胞治療β地中(zhōng)海貧血試驗處于早期1期臨床試驗階段,未有(yǒu)其他(tā)進展,官方網站也未查詢到相關管線(xiàn)信息。

▲圖片來源:https://www.clinicaltrials.gov
(8)上海本導基因技(jì )術有(yǒu)限公(gōng)司
本導基因成立于2018年,是一家基因治療創新(xīn)藥物(wù)開發的企業,擁有(yǒu)mRNA遞送與基因編輯平台、第四代慢病毒載體(tǐ)平台、溶瘤病毒平台,主要用(yòng)于治療糖尿病黃斑變性、濕性老年黃斑變性(wAMD)

、造血系統遺傳疾病等疾病。本導基因的基因添加——BDlenti平台使用(yòng)先進的慢病毒載體(tǐ)遞送技(jì )術,有(yǒu)效地提高了病毒産(chǎn)量以及造血幹細胞的感染效率。BDlenti遞送技(jì )術加入了獨特的優化策略,可(kě)以降低基因整合突變的風險。同時,讓治療性基因在患者體(tǐ)内長(cháng)期表達,而不會因為(wèi)基因沉默而失掉療效。▲
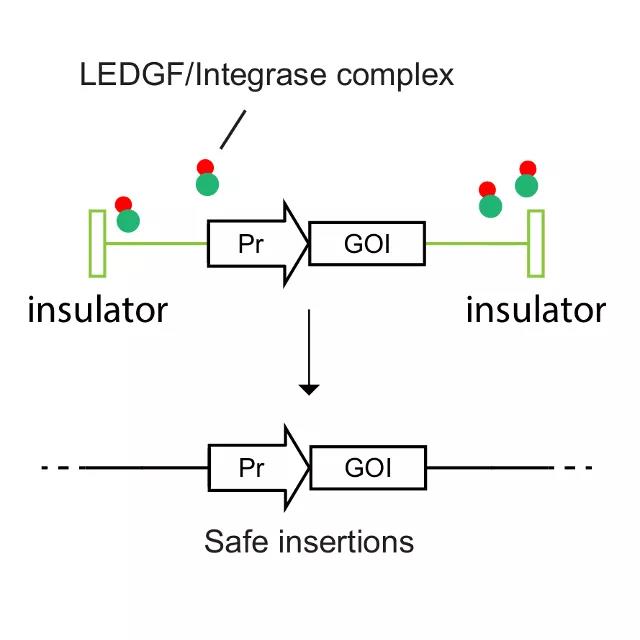
圖片來源:本導基因官方網站
基于BDlenti遞送技(jì )術,本導基因開發了治療地中(zhōng)海貧血症的基因療法BD211,目前也是公(gōng)司開發的産(chǎn)品管線(xiàn)中(zhōng)進展較快的基因療法之一,适應症還包括鐮刀(dāo)形紅細胞貧血症,但目前僅處于技(jì )術開發階段。此外,本導基因還在2020年6月完成了千萬級人民(mín)币的pre-A輪融資,用(yòng)于推進基于mRNA遞送的基因治療産(chǎn)品的臨床應用(yòng)。
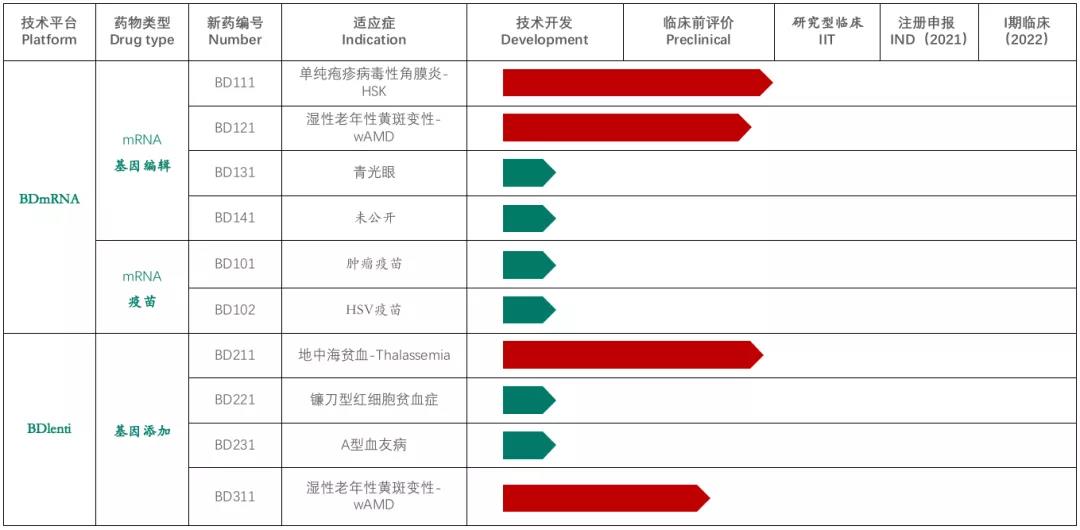
▲圖片來源:本導基因官方網站
(9)上海邦耀生物(wù)科(kē)技(jì )有(yǒu)限公(gōng)司
上海邦耀生物(wù)科(kē)技(jì )有(yǒu)限公(gōng)司成立于2013年,依托在基因編輯、免疫學(xué)領域的強大技(jì )術實力和科(kē)研團隊,緻力于基因編輯與細胞治療的研發與轉化,以及基因突變引起的遺傳疾病的基因治療。

邦耀生物(wù)已搭建基因編輯、細胞治療與基因治療三大具(jù)有(yǒu)自主知識産(chǎn)權的技(jì )術平台,其中(zhōng)基因編輯治療β 地中(zhōng)海貧血症、PD1定點整合的非病毒CART、以及UCART等項目已經取得優異臨床效果。
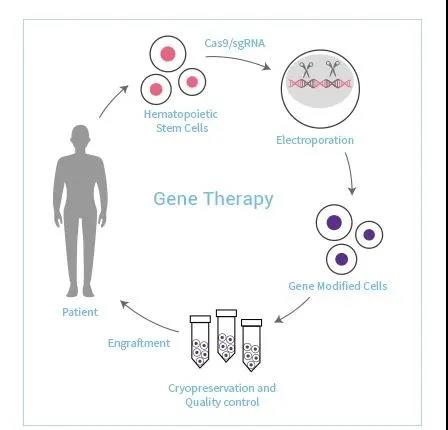
▲圖片來源:邦耀生物(wù)官方網站
2019年3月,Nature Medicine在線(xiàn)發表了邦耀生物(wù)關于基因編輯療法用(yòng)于地貧治療的研究成果。結果表明,通過CRISPR/Cas9技(jì )術重新(xīn)開啓胎兒期的γ珠蛋白的表達,從而代替有(yǒu)缺陷的β珠蛋白,達到緩解地貧症狀的目的,具(jù)有(yǒu)很(hěn)大的臨床轉化潛力。
(10)廣州瑞風生物(wù)科(kē)技(jì )有(yǒu)限公(gōng)司
瑞風生物(wù)成立于2019年,是一家以基因編輯為(wèi)核心技(jì )術的藥物(wù)創新(xīn)企業,目前處于臨床前階段。

基于革新(xīn)性的基因編輯技(jì )術,瑞風生物(wù)目前在遺傳病、複雜疾病和腫瘤領域等皆有(yǒu)管線(xiàn)布局,其中(zhōng)進展最快的β-地中(zhōng)海貧血基因編輯療法。

▲圖片來源:瑞風生物(wù)官方網站
除制藥企業之間的合作(zuò),還有(yǒu)醫(yī)院與企業合作(zuò)共同開發β地中(zhōng)海貧血基因療法,如廣州南方醫(yī)院與廣東銥科(kē)基因科(kē)技(jì )有(yǒu)限公(gōng)司共同申報一項基因治療重症β地中(zhōng)海貧血的研究(NCT03276455),銥科(kē)基因是賽爾生物(wù)的控股子公(gōng)司,首席研究員李春富博士有(yǒu)“中(zhōng)國(guó)地貧之父”之稱,目前該研究處于1/2期臨床研究階段;意大利IRCCS San Raffaele醫(yī)院使用(yòng)GLOBE慢病毒載體(tǐ)轉導自體(tǐ)HSC的策略,與Orchard等共同申報的β 地中(zhōng)海貧血基因治療臨床試驗正處于I/II期臨床試驗階段(NCT02453477),這也是第一個同時應用(yòng)于成人和兒科(kē)患者的β 地中(zhōng)海貧血基因治療臨床試驗。
3、基因療法用(yòng)于鐮狀細胞病
鐮狀細胞病(Sickle Cell Disease,SCD)是一組由β-珠蛋白基因突變引起的遺傳性紅細胞疾病。正常情況下,健康的紅細胞呈圓盤狀,易于在血管中(zhōng)移動,将氧氣輸送至身體(tǐ)的各個部位,但基因突變所導緻的鐮狀紅細胞阻礙血液流動,從而引發貧血等其他(tā)嚴重問題,特别是血管阻塞性危象(vaso-occlusive crises,VOC)。VOC也被稱為(wèi)鐮狀細胞疼痛危象(sickle cell pain crisis,SCPC),是由多(duō)細胞粘附或阻斷血流的細胞簇所觸發,可(kě)導緻嚴重的急性和慢性危及生命的并發症和死亡。它是SCD患者急診室就診和住院的最常見原因,在SCD患者中(zhōng),當多(duō)個血細胞粘在一起并黏附在血管上時,VOC就會發生,導緻阻塞,但是目前能(néng)夠預防VOC的方案也非常有(yǒu)限。
目前,針對SCD的治療方法包括藥物(wù)治療、輸血和幹細胞移植。
最早被批準用(yòng)于治療鐮狀細胞疾病的藥物(wù)是Hydroxyurea(羟基脲),但該藥物(wù)隻能(néng)用(yòng)來緩解症狀,并不能(néng)治愈;2017年,Emmaus Medical公(gōng)司研發的Endari(L-谷氨酰胺口服粉劑)被FDA批準用(yòng)于治療5歲及以上的SCD患者,有(yǒu)助于限制血管阻塞性危象的持續時間、嚴重程度和發生頻率;2019年,有(yǒu)兩款治療SCD的藥物(wù)獲得FDA的上市批準,分(fēn)别是諾華研發的Adakveo(Crizanlizumab)與Global Blood Therapeutics(GBT)研發的Oxbryta(Voxelotor),Crizanlizumab是首款獲批治療VOC的靶向療法,2020年在歐洲也獲得了批準;但目前這兩款藥均未在國(guó)内獲批。幹細胞移植法可(kě)以治愈SCD,但是供體(tǐ)來源有(yǒu)限,在臨床上也有(yǒu)諸多(duō)局限。
2017年,國(guó)際權威醫(yī)學(xué)期刊《新(xīn)英格蘭醫(yī)學(xué)雜志(zhì)》(NEJM)上發表了一項研究成果,通過基因治療“治愈”了一位15歲鐮狀細胞病患者。能(néng)徹底治愈SCD的基因療法被寄予厚望,目前大家也在進行積極的嘗試。
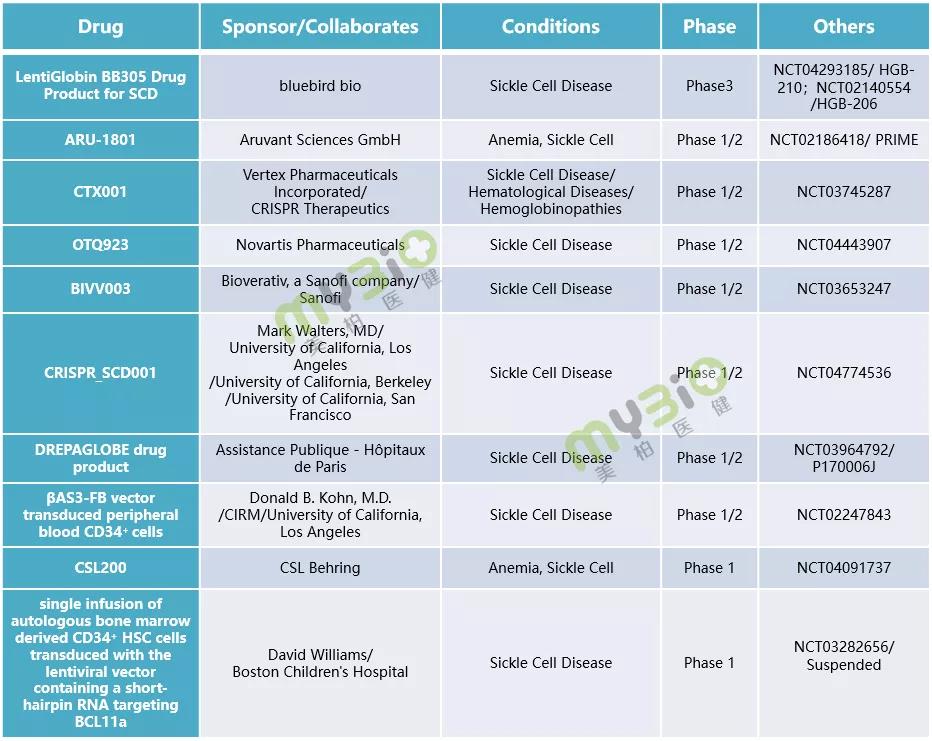
▲表3 處于臨床階段的部分(fēn)鐮狀細胞病基因治療
數據來源:https://www.clinicaltrials.gov
基因療法區(qū)别于傳統小(xiǎo)分(fēn)子、單雙抗藥物(wù)等治療方式,在治療具(jù)有(yǒu)遺傳性的血液疾病上具(jù)有(yǒu)獨特的優勢,大多(duō)數公(gōng)司在開展試驗研究時可(kě)能(néng)也不止選擇一個适應症。如同一種基因療法可(kě)能(néng)會應用(yòng)于治療地中(zhōng)海貧血與鐮狀細胞病中(zhōng),前者是應用(yòng)基因療法技(jì )術改變血紅蛋白結構,後者是改變細胞形狀。
研發基因療法用(yòng)于治療鐮狀細胞病的代表公(gōng)司:
(1)Aruvant Sciences
瑞士生物(wù)制藥公(gōng)司Roivant Sciences的子公(gōng)司Aruvant Sciences是一家臨床階段生物(wù)制藥公(gōng)司,緻力于開發針對罕見疾病的變革性療法并将其商(shāng)業化。

Aruvant的主要候選産(chǎn)品ARU-1801是一種針對SCD的個體(tǐ)潛在治愈型慢病毒基因療法,目前正處在臨床試驗階段。作(zuò)為(wèi)一次性治療SCD的基因療法,ARU-1801目前已經獲得FDA治療SCD的罕見兒科(kē)疾病資格認定(RPD)和孤兒藥資格(ODD)以及EMA授予的優先藥品資格(PRIME)。
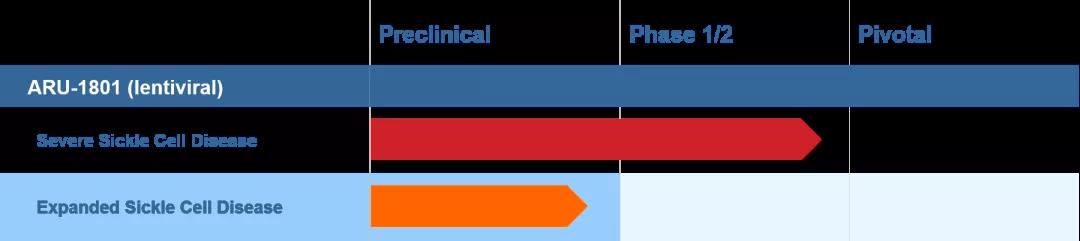
▲圖片來源:Aruvant 官方網站
(2)CSL Behring
CSL Behring是澳洲最大上市醫(yī)療公(gōng)司、全球血液制品巨頭CSL的子公(gōng)司。上文(wén)在介紹UniQure的血友病管線(xiàn)時也提到,CSL Behring與UniQure就B型血友病患者的基因治療産(chǎn)品達成合作(zuò),早前CSL Behring也曾收購(gòu)美國(guó)生物(wù)科(kē)技(jì )公(gōng)司Calimmune及其專有(yǒu)的體(tǐ)外造血幹細胞基因治療平台,其造血幹細胞基因療法便是用(yòng)于治療鐮狀細胞疾病及b地中(zhōng)海貧血。

CSL Behring研發管線(xiàn)中(zhōng),除治療SCD的基因療法CSL200外,也有(yǒu)血漿衍生血紅素療法CSL889,該療法也獲得了歐盟委員會和FDA的孤兒藥資格認定。此外,還有(yǒu)已上市的治療A型血友病的AfstylaÒ與治療B型血友病的IdelvionÒ。

▲圖片來源:CSL Behring官方網站
(2)Graphite Bio
Graphite Bio創立于2019年,是一家美國(guó)基因編輯技(jì )術服務(wù)商(shāng),Graphite的技(jì )術方法基于其科(kē)學(xué)聯合創始人Matthew Porteus博士和Maria Grazia Roncarolo博士的學(xué)術成果,Matthew Porteus博士同時也是CRISPR Therapeutics的科(kē)學(xué)創始人。Graphite成立時間雖短,但已經進行了兩輪融資,在2021年的3月15日,Graphite完成了1.5億美元的B輪融資,此前完成4500萬美元的A輪融資。

Graphite Bio主要利用(yòng)基因編輯與造血幹細胞移植技(jì )術進行療法開發。目前,Graphite管線(xiàn)上已經有(yǒu)6款在研基因療法,适應證包括SCD、X連鎖重症聯合免疫缺陷病和戈謝(xiè)病等。2020年12月,Graphite宣布,治療SCD的候選藥物(wù)GPH101的IND申請已獲FDA批準,首個臨床I/II期試驗即将啓動,Graphite計劃2021年初開始招募CEDAR臨床試驗,也讓我們期待這項試驗結果(clinicaltrials.gov上尚未收錄)。
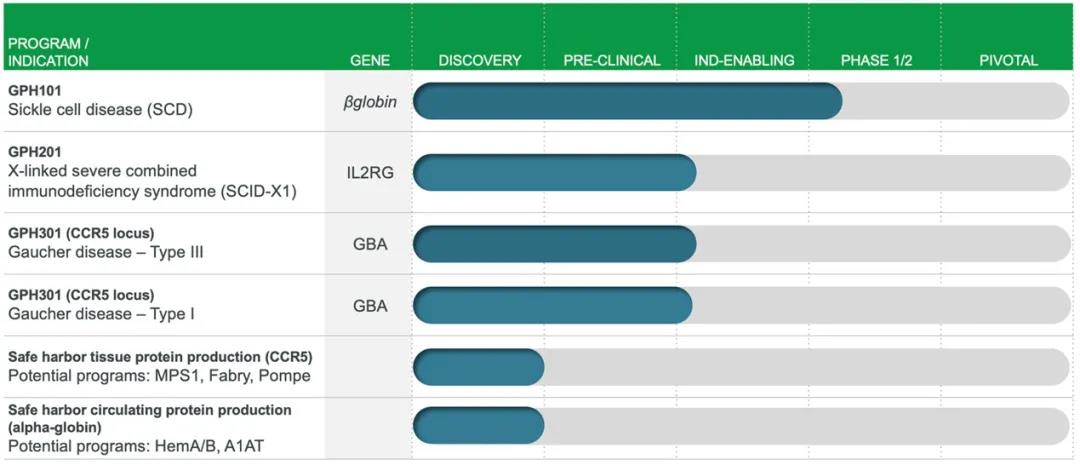
▲圖片來源:Graphite 官方網站
(3)Intellia Therapeutics/Novartis
Intellia公(gōng)司成立于2014年,公(gōng)司創始人詹妮弗·杜德(dé)娜(Jennifer Doudna)獲得 2020 諾貝爾化學(xué)獎,是CRISPR基因編輯領域的權威人士。

OTQ923/HIX763是Intellia與Novartis合作(zuò)開發的一種基于CRISPR/Cas9基因組編輯的造血幹細胞(HSCs)療法,用(yòng)于治療SCD。Novartis對于基因治療領域也在積極布局,2018年,Novartis以87億美金收購(gòu)基因治療公(gōng)司AveXis,并獲得全球首個治療SMA的基因治療産(chǎn)品Zolgensma;2020年,Novartis又(yòu)以2.8億美元收購(gòu)Vedere Bio公(gōng)司,并獲得其全套的眼科(kē)疾病基因治療平台,擴大在基因治療和細胞療法領域的優勢。目前,Novartis在基因領域有(yǒu)4項臨床項目、19個臨床前項目。

▲圖片來源:Intellia官方網站
(4)Beam Therapeutics
Beam成立于2017年,是首家利用(yòng)單堿基編輯技(jì )術開發精(jīng)準基因藥物(wù)的生物(wù)技(jì )術公(gōng)司,由張鋒教授、David Liu教授以及J. Keith Joung教授共同創立。2020年2月,Beam在納斯達克上市,IPO當日募集超1.8億美元;2021年2月,Beam宣布,以1.2億美元收購(gòu)用(yòng)于基因療法的非病毒載體(tǐ)遞送工(gōng)具(jù)的開發商(shāng)Guide Tx,加碼基因療法研究。

在Beam的産(chǎn)品管線(xiàn)上我們能(néng)看到,暫時還未有(yǒu)在研候選産(chǎn)品進入臨床試驗階段。Beam用(yòng)于治療血液疾病的基因療法BEAM-101和BEAM-102是基于電(diàn)穿孔技(jì )術,将基礎編輯工(gōng)具(jù)插入從患者體(tǐ)内提取的細胞中(zhōng),以治療TDT和SCD,預計會在2021年内開始第一次人體(tǐ)臨床試驗。
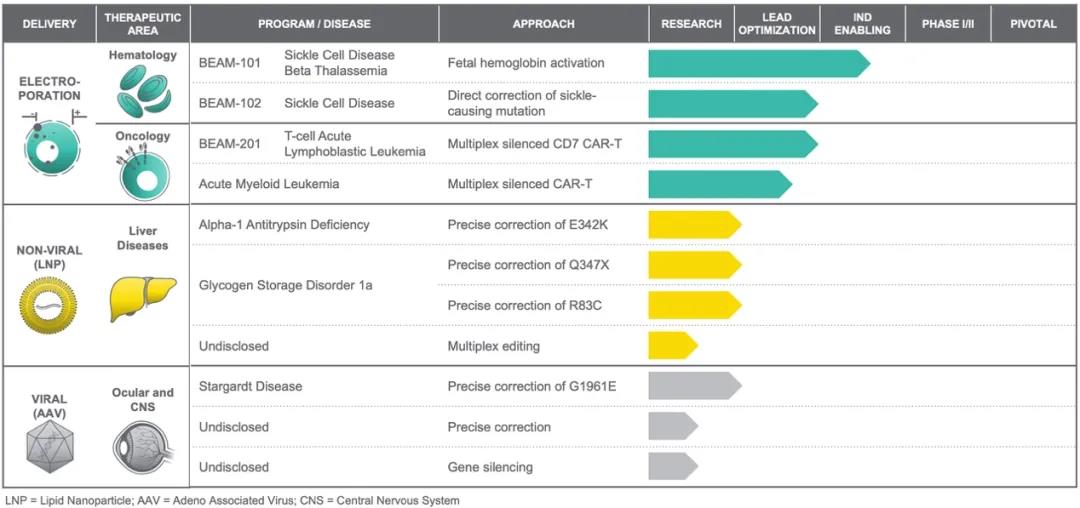
▲圖片來源:Beam官方網站
加利福尼亞大學(xué)Mark研究了一種治療SCD的療法 CRISPR_SCD001,該療法使用(yòng)CRISPR/Cas9編輯過的造血幹細胞(稱之為(wèi)CRISPR_SCD001藥品)進行移植(HSCT)。另外還有(yǒu)像上文(wén)中(zhōng)提到的bluebird bio、CRISPR Therapeutics、Editas Medicine、本導基因等制藥企業、科(kē)研院校及機構也在積極開發SCD的基因療法。
4、基因治療用(yòng)于範可(kě)尼貧血
範可(kě)尼貧血(Fanconi anemia,FA)是一種罕見的常染色體(tǐ)隐性遺傳性血液系統疾病,與DNA鏈間鉸鏈修複缺陷而引起的染色體(tǐ)不穩定有(yǒu)關。除典型的血液系統症狀之外,還可(kě)能(néng)伴随骨骼畸形、性發育不全等,甚至可(kě)導緻嚴重的并發症如骨髓衰竭、急性髓樣白血病(AML)、骨髓增生異常綜合症(MDS)等。2018年5月國(guó)家衛健委公(gōng)布的《第一批罕見病目錄》中(zhōng),範可(kě)尼貧血與地中(zhōng)海貧血均被收錄。
對于範可(kě)尼貧血的第一線(xiàn)治療是雄性激素療法和造血生長(cháng)因子療法,但是隻有(yǒu)50%-75%的患者對藥物(wù)治療有(yǒu)反應。雄激素療法代表藥如羟甲烯龍(oxymetholone),在治療中(zhōng)通常是羟甲烯龍聯合較小(xiǎo)量潑尼松,但在治療期間要注意肝功損害等毒副作(zuò)用(yòng)問題;造血生長(cháng)因子如G-CSF和GM-CSF能(néng)改善造血,特别是對于中(zhōng)性粒細胞減少的患者,能(néng)增加其中(zhōng)性粒細胞絕對值,代表藥如首款口服血小(xiǎo)闆生成素艾曲泊帕(Eltrombopag,Promacta,Revolade)。
造血幹細胞移植法(HSCT),特别是HLA匹配同胞供者異基因造血幹細胞移植法(MSDallo-HSCT)是治療範可(kě)尼貧血最有(yǒu)效方法,不僅能(néng)夠治愈範可(kě)尼貧血患者,也能(néng)預防并發症白血病的發生,但仍需要面對供體(tǐ)來源的問題。目前,基因治療的研究正在火熱進行中(zhōng),臨床上也亟需為(wèi)範可(kě)尼貧血患者開發更有(yǒu)效的療法。
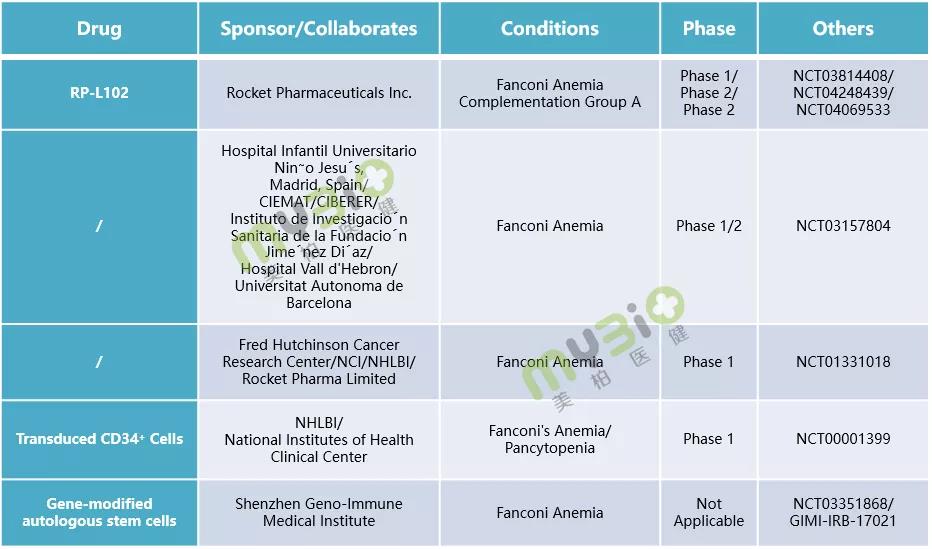
▲表4 處于臨床階段的部分(fēn)範可(kě)尼貧血基因治療候選療法
數據來源:https://www.clinicaltrials.gov
相對于其他(tā)的遺傳性血液疾病如血友病、地中(zhōng)海貧血等,基因療法用(yòng)于範可(kě)尼貧血的研究相對較少,但這也并不影響我們從科(kē)學(xué)理(lǐ)論的角度出發,去相信基因療法會成為(wèi)範可(kě)尼貧血等疾病的終結者。
研發基因療法用(yòng)于治療範可(kě)尼貧血的代表公(gōng)司:
(1)Rocket Pharma
Rocket是一家多(duō)平台基因治療公(gōng)司,應用(yòng)成熟的慢病毒載體(tǐ)(LVV)和腺相關病毒載體(tǐ)(AAV)基因治療平台,開發罕見的、毀滅性疾病的基因療法。

Rocket現有(yǒu)5項基因治療候選産(chǎn)品,其中(zhōng)4項基于LVV平台所開發,1項基于AVV平台。目前進展最快的是用(yòng)于治療範可(kě)尼貧血的基因療法RP-L102和用(yòng)于促進白細胞粘附的基因療法RP-L201。其他(tā)的基因療法包括治療Danon病的RP-A501、治療丙酮酸激酶缺乏症(PKD)的RP-L301以及治療小(xiǎo)兒惡性骨硬化病(IMO)的RP-L401也均處在臨床試驗研究階段。
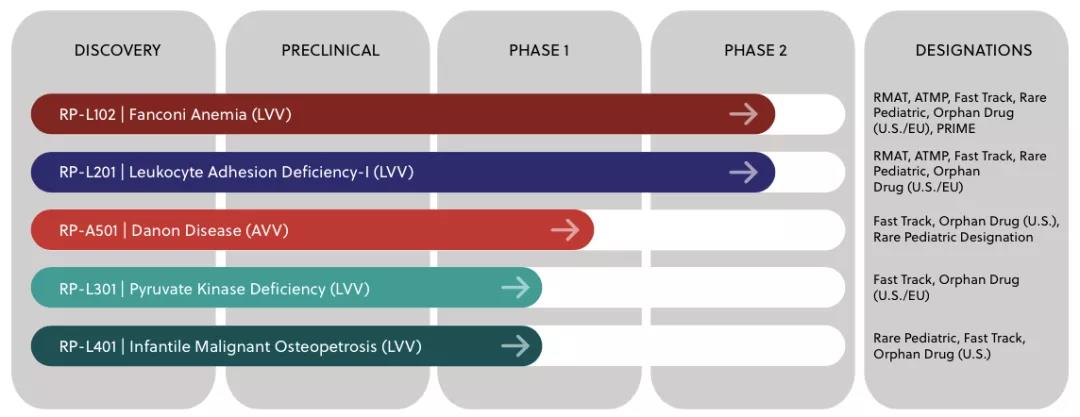
▲圖片來源:Rocket官方網站
(2)Stridebio
StrideBio成立于2015年,是一家專注于開發基于腺相關病毒(AAV)基因療法的公(gōng)司。StrideBio于2018年獲得1570萬美元的A輪融資,在2021年3月,StrideBio又(yòu)完成超額認購(gòu)的B輪融資8150萬美元,該資金将用(yòng)于進一步優化公(gōng)司産(chǎn)品管線(xiàn)。

StrideBio利用(yòng)其專有(yǒu)的STRIVE™平台,設計改造AAV載體(tǐ),以呈現獨特的AAV衣殼,改進基因療法的組織特異性、轉導效率等。基于該技(jì )術,StrideBio與Takeda、Sarepta等公(gōng)司展開合作(zuò),管線(xiàn)中(zhōng)進展最快的是治療範可(kě)尼貧血的基因療法STRX-110與治療尼曼匹克症C型的STRX-210。
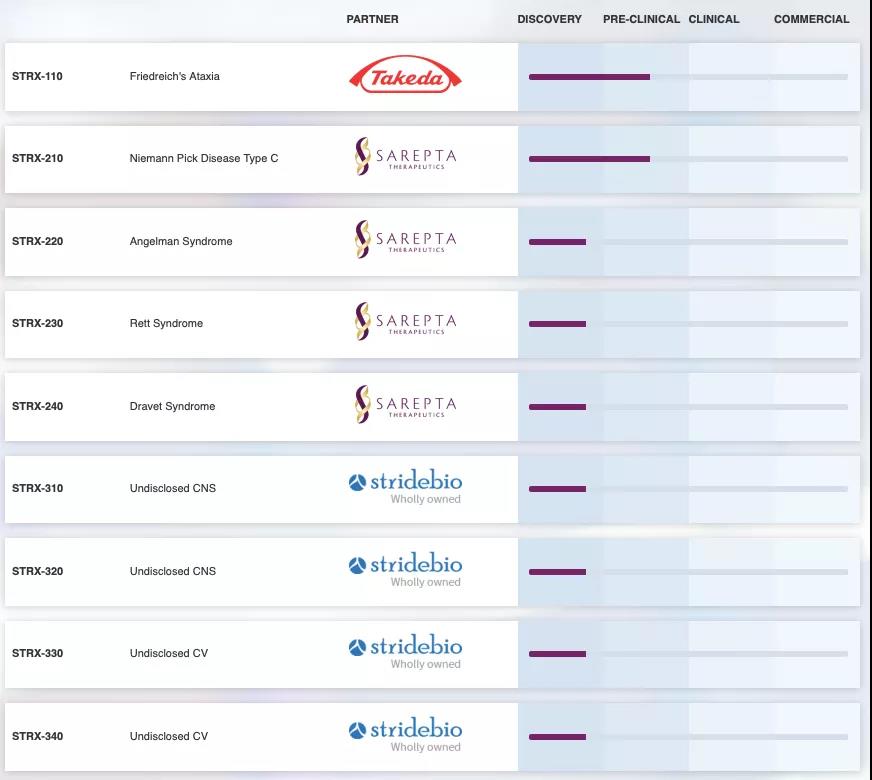
▲圖片來源:Stridebio官方網站
另有(yǒu)消息稱,Abeona公(gōng)司曾采用(yòng)一種新(xīn)型的基于CRISPR/Cas9基因編輯方法的療法ABO-301(AAV-FANCC)用(yòng)于治療範可(kě)尼貧血,但目前在該公(gōng)司的研發管線(xiàn)中(zhōng)并未看到ABO-301的研究進展,其他(tā)渠道也未查到相關信息。
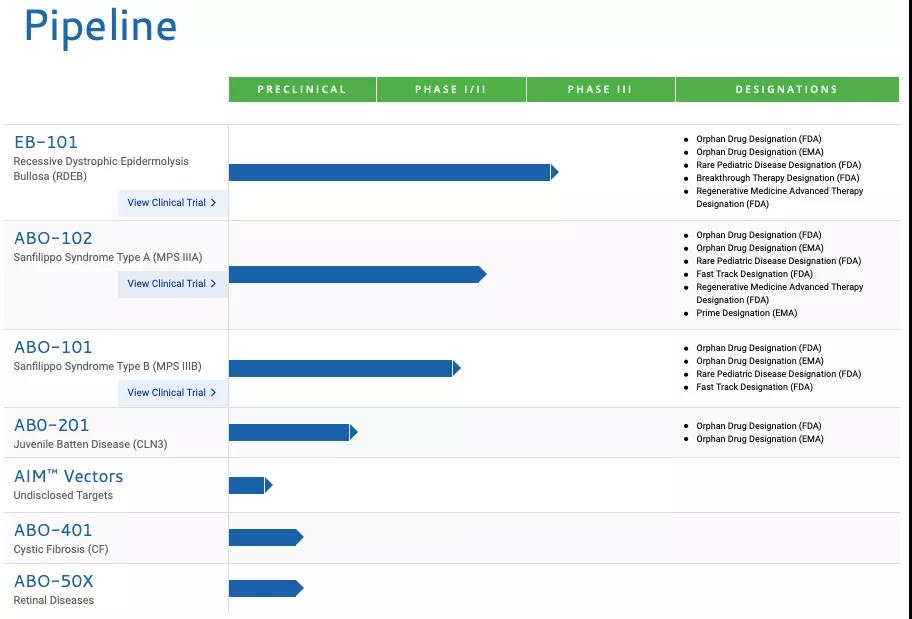
▲圖片來源:Abeona官方網站
國(guó)内研究範可(kě)尼貧血進入臨床階段的是深圳市免疫基因治療研究院,目前正在招募志(zhì)願者中(zhōng),這也該研究院基因治療血液遺傳疾病的第三個研究方向。

▲圖片來源:深圳市免疫基因治療研究院官方網站
基因療法除能(néng)用(yòng)于治療血友病、地中(zhōng)海貧血、鐮狀細胞病及範可(kě)尼貧血等遺傳性血液疾病外,也有(yǒu)研究者利用(yòng)基因技(jì )術治療血液腫瘤。
緻力于異體(tǐ)CAR-T療法開發的法國(guó)生物(wù)公(gōng)司Cellectis開發了一款用(yòng)于治療急性髓系白血病(Acute myeloid leukemia,AML)的UCART123,該療法通過TALEN技(jì )術基因編輯異體(tǐ)T細胞,使之特異性靶向AML和母細胞性漿細胞樣樹突狀細胞腫瘤(Blastic Plasmacytoid Dendritic CellNeoplasm,BPDCN)細胞表面的CD123抗原而發揮作(zuò)用(yòng)。2017年2月,UCART123獲得美國(guó)FDA的IND批準,用(yòng)于治療成為(wèi)第一款由FDA批準進入臨床試驗的此類産(chǎn)品,但UCART123後續的臨床試驗并不順利。同年9月,臨床試驗中(zhōng)便出現了一個BPDCN的患者死亡事件,随後就被FDA叫停,并要求Cellectis在安(ān)全性上重新(xīn)設計,2個月後FDA才恢複該療法的臨床試驗,根據clinicaltrials.gov顯示,目前該療法仍處于1期臨床試驗階段。
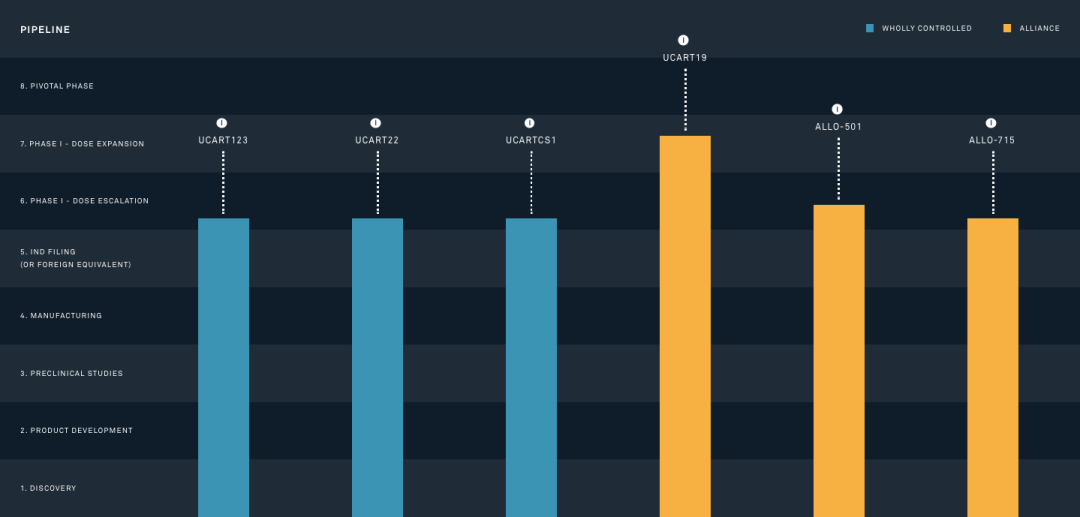
▲圖片來源:Cellectis官方網站
不僅是Cellectis公(gōng)司,Precision BioSciences/施維雅也開發了CD19導向、同種異體(tǐ)嵌合抗原受體(tǐ)T細胞療法(CAR-T)PBCAR0191,用(yòng)來治療晚期B細胞前體(tǐ)急性淋巴細胞白血病(B-ALL)。Precision通過其專有(yǒu)的ARCUS®基因組編輯平台在體(tǐ)外對T細胞進行修飾,在T細胞受體(tǐ)(TCR)位點插入CAR基因并同時敲除TCR,進行體(tǐ)外擴增後再回輸至患者體(tǐ)内以達到治療目的。基于該平台技(jì )術,Precision也構建了包括多(duō)個通用(yòng)型CAR-T免疫細胞療法和數個體(tǐ)内基因校正療法的管線(xiàn)。2019年3月,PBCAR0191正式開啓了1期臨床試驗,适應症包括B-ALL和非霍奇金淋巴瘤,根據clinicaltrials.gov顯示,目前該療法處于1/2期臨床試驗階段。
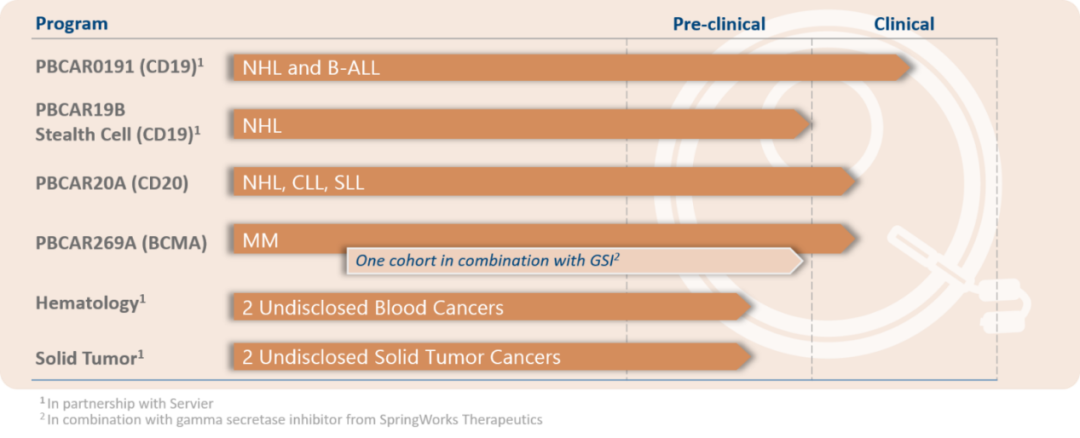
▲圖片來源:Precision官方網站
除上述Biotech之外,越來越多(duō)的大型制藥公(gōng)司正在積極投入到基因療法的布局中(zhōng),通過并購(gòu)、合作(zuò)開發等方式介入這一領域,獲得強勁的競争力量。像文(wén)中(zhōng)提到的輝瑞、賽諾菲、諾華等公(gōng)司就在血友病、地中(zhōng)海貧血等血液疾病領域與基因治療公(gōng)司合作(zuò)開發。
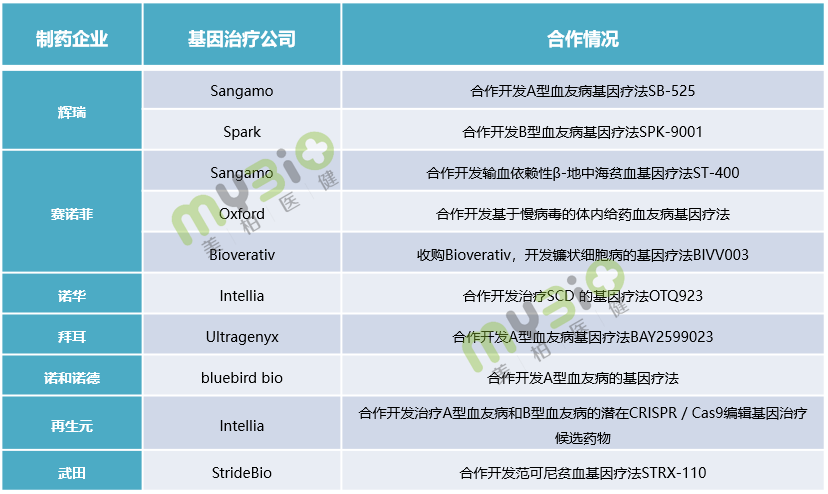
▲表5 部分(fēn)大型制藥企業在血液遺傳病領域的合作(zuò)情況
綜合來看,國(guó)外的基因治療行業大步向前,國(guó)内的企業也在快速追趕。就本篇内容分(fēn)析,全球開展基因治療血液遺傳疾病臨床試驗研究最多(duō)的國(guó)家是美國(guó),大概占比65%,中(zhōng)國(guó)也在積極開展,占比近20%,其他(tā)國(guó)家如英國(guó)、意大利、西班牙、法國(guó)等也在進行血液疾病的臨床研究,但與美國(guó)和中(zhōng)國(guó)相比還是較為(wèi)落後;并且,這些研究與開發血液遺傳病基因療法的企業一半也是注冊在美國(guó),還有(yǒu)約三分(fēn)之一是中(zhōng)國(guó)企業,我國(guó)的基因行業正逐漸興起。目前,美國(guó)的基因治療進展仍穩居首位,我國(guó)雖緊随其後,但也有(yǒu)一定的距離,這有(yǒu)可(kě)能(néng)是長(cháng)久以來,兩國(guó)在生物(wù)領域這一大闆塊上科(kē)研和技(jì )術的水平、臨床治療經驗的積累以及政策監管的實施和投入等多(duō)方面差距導緻的。
在血液遺傳病的基因治療領域,僅有(yǒu)治療β 地中(zhōng)海貧血的Zynteglo獲EMA批準有(yǒu)條件上市,其他(tā)進展較快的、有(yǒu)希望緊随其後上市的屬适應症為(wèi)SCD的Zynteglo(β 地中(zhōng)海貧血獲批)、BioMairn的BMN270、Sangamo/輝瑞的SB-525,這些産(chǎn)品均處于3期臨床試驗階段。國(guó)内基因治療領域的研究雖在數目上比較樂觀,但臨床研究基本處在臨床前或1期臨床試驗階段,不過國(guó)内的監管部門也随着這一技(jì )術的快速發展而不斷出台新(xīn)的相關政策,以更加規範、全面的實施監管。基因療法也許會成為(wèi)中(zhōng)國(guó)實現彎道超車(chē),拉近與國(guó)外生物(wù)技(jì )術水平距離的機會。在2020年10月,我國(guó)也迎來了首個CRISPR基因編輯療法臨床試驗申請,這一裏程碑事件也會激勵着越來越多(duō)國(guó)内新(xīn)興技(jì )術的企業取得革命性的突破。
基因療法能(néng)夠從“根本”去解決問題,所以,該治療方案被認為(wèi)有(yǒu)望治愈傳統藥物(wù)不能(néng)解決的疾病。對于如血友病、地中(zhōng)海貧血、鐮狀細胞病等的血液遺傳疾病,基因療法是較為(wèi)理(lǐ)想治療方案,通過改造缺陷基因達到徹底治愈疾病的目的;其他(tā)比較熱門的适應症還包括遺傳性眼部疾病如遺傳性視網膜疾病、遺傳性視神經病變等。随着技(jì )術的進步,基因療法将會在越來越多(duō)的适應症上展現良好的治療效果,我們應持續關注該領域的發展。
----------THE END----------
免責聲明:本文(wén)系轉載分(fēn)享,文(wén)章觀點、内容、圖片及版權歸原作(zuò)者所有(yǒu),如涉及侵權請聯系删除!



































































